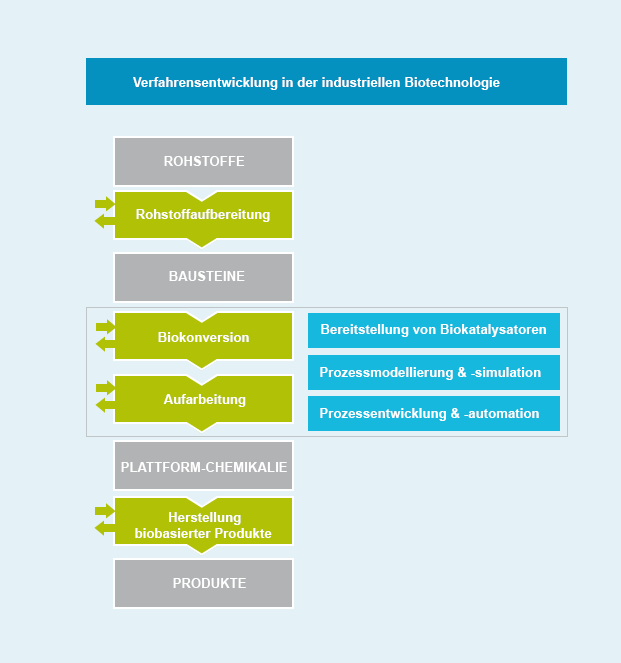
Verfahrensentwicklung in der industriellen Biotechnologie
Gute Praxis
Definition von industrieller Biotechnologie
In der industriellen Biotechnologie (Weiße Biotechnologie) werden solche Anwendungen erforscht und in technologieorientierten Verfahren umgesetzt, in denen mit Hilfe von lebenden Organismen und Teilen von diesen (z. B. Enzyme) diverse Produkte hergestellt werden. Zahlreiche Produkte wie hochwertige Chemikalien, Enzyme, Vitamine, Wasch-und Reinigungsmittel, Lebensmittel, Agrochemikalien sowie Arzneimittel werden mit Hilfe biotechnologischer Verfahren hergestellt [biotechnologie.de c/o BIOCOM AG (2019)].
Durch die Ausnutzung biologischer Prozesse und Strukturen („Werkzeugkasten der Natur“) sollen Güter des alltäglichen Lebens ressourcenschonender und nachhaltiger produziert werden. Da in vielen Fällen biobasierte und nachwachsende Rohstoffe als Eingangsstoffstrom in den industriellen biotechnologischen Verfahren eingesetzt werden, schont dies die endlich zur Verfügung stehenden Rohstoffe wie Erdöl und Kohle [biotechnologie.de c/o BIOCOM AG (2019)], [Schüler, J. (2016), S. 134].
Für immer mehr Nationen stellt eine biobasierte Ökonomie ein anzustrebendes Ziel in der Zukunft dar. Dabei wird zukünftig ein Verzicht auf die Verwendung nichterneuerbarer Ressourcen sowie die Produktion toxischer Abfälle angestrebt [Schüler, J. (2016), S. 288].
Quelle(n):
- biotechnologie.de c/o BIOCOM AG (2019): Was ist Biotechnologie? [online]. BIOCOM AG [abgerufen am: 20.12.2019], verfügbar unter: Link
- Schüler, J. (2016): Die Biotechnologie-Industrie, Springer Berlin Heidelberg, ISBN 978-3-662-47159-3.
Herausforderungen und Lösungsansätze in der Bioprozessentwicklung
Die Entwicklung neuer Bioprozesse ist geprägt von wirtschaftlichen Unsicherheiten. Diese ergeben sich aufgrund [Wiechert, W. et al. (2018), S. 10]
- einer sehr schwierigen Einschätzung von Realisierbarkeit, Produktivität und Konkurrenzfähigkeit (Grund: volatile Märkte),
- schwer vorhersagbarer Zeiten für die Entwicklung von Prozessen und Produkten,
- einer (möglichen) variierenden Rohstoffbasis, die einen hohen Bedarf an Verfahrensflexibilität nach sich zieht.
Um diese Herausforderungen zu meistern, bedarf es Lösungskonzepten wie Miniaturisierung, Automatisierung und Digitalisierung. Bereits heute ist eine beschleunigte Bioprozessentwicklung mittels des Einsatzes von Hochdurchsatzverfahren in Verbindung mit bioinformatischen Algorithmen möglich. Zukünftige Entwicklungen in folgenden Technologiebereichen könnten dazu beitragen, die bestehenden Risiken und Herausforderungen in der Bioprozessentwicklung zu überwinden und zu meistern. Dies trägt dazu bei, dass die Entwicklung von Bioprozessen nicht abschreckend auf Unternehmen wirkt und sich dementsprechend immer mehr Unternehmen für eine Entwicklung und Umsetzung entscheiden [Wiechert, W. et al. (2018), S. 10]:
- Durchsatzsteigerung in der Verfahrensentwicklung (Labor) aufgrund von hochauflösender Analytik und Hochdurchsatzverfahren (parallele Experimente)
- Hohes Effizienzpotenzial durch miniaturisierte Produktionsverfahren mittels Mikrosystemtechnik wie Mikroreaktoren, Mikro-Sensoren oder miniaturisierten Analytiksystemen
- Enorme Synergieeffekte durch Werkzeugintegration
Quelle(n):
- Wiechert, W.; Scheper, T. und Weuster-Botz, D. (2018): Neue Schubkraft für die Biotechnologie – Miniaturisierung, Automatisierung und Digitalisierung revolutionieren die Entwicklung biotechnologischer Prozesse und Produkte. DECHEMA Gesellschaft für Chemische Technik und Biotechnologie e.V., Frankfurt am Main [abgerufen am: 12.12.2019], verfügbar unter: Link
Kombinierte Entwicklung von Labor- und Produktionsprozessen
In der weißen Biotechnologie waren bisher die Verfahrensentwicklung in Laboranlagen und der eigentliche Produktionsprozess weitestgehend voneinander getrennt. Nur in Laboranlagen wurde eine ausreichende Datenmenge erzeugt, die für eine Entwicklung des Produktionsverfahrens ausreichte. Mit zunehmender Digitalisierung, auch in biotechnologischen Produktionsverfahren, steigt die Anzahl an Messsensoren im Produktionsprozess. Dadurch wird eine hohe Dichte an Prozessdaten erzeugt. Eine kontinuierliche integrierte Verbesserung und Weiterentwicklung des laufenden Prozesses werden dadurch zukünftig möglich. Die Entwicklungszeit sowie der Material- und Energieaufwand im Labor werden in Zukunft geringer ausfallen [Wiechert, W. et al. (2018), S. 8].
Quelle(n):
- Wiechert, W.; Scheper, T. und Weuster-Botz, D. (2018): Neue Schubkraft für die Biotechnologie – Miniaturisierung, Automatisierung und Digitalisierung revolutionieren die Entwicklung biotechnologischer Prozesse und Produkte. DECHEMA Gesellschaft für Chemische Technik und Biotechnologie e.V., Frankfurt am Main [abgerufen am: 12.12.2019], verfügbar unter: Link
Motivation für einen Einsatz industrieller biotechnologischer Verfahren
Die Hauptmotivation für die Entwicklung und den Einsatz industriell biotechnologischer Verfahren ist die Realisierung einer sauberen, umwelt- und klimaschonenden Produktionsweise. Die hiermit verfolgten Ziele beinhalten die Absenkung von Investitions-, Energie- und Entsorgungskosten, die Verringerung der Abhängigkeit von fossilen Rohstoffen sowie die Entwicklung neuer Produkte und Systemlösungen. Die Erreichung dieser Ziele führt in der Regel auch zu einer Erhöhung der Wettbewerbsfähigkeit der jeweiligen Unternehmen [Kagermann, H. et al. (2017), S. 39], [biotechnologie.de c/o BIOCOM AG et al. (2015), S. 4 ff.].
Die gesamte Bandbreite der möglichen Vorteile (ökonomisch, ökologisch, funktionell) industriell biotechnologischer Verfahren ist im Folgenden zusammenfassend aufgeführt [Schüler, J. (2016), S. 257 und S. 288], [Braun, M. et al. (2006), S. 57]:
| Vorteile | ||
| Funktionell | Ökologisch | Ökonomisch |
| Weniger Synthese- und Aufbereitungsschritte | Geringerer Rohstoffeinsatz | Geringere Investitionskosten |
| Milde Reaktionsbedingungen (z. B. geringere Temperaturen, Drücke und pH-Werte) | Geringerer Wasserverbrauch | Geringere Betriebskosten (Rohstoffe, Wasser, Energie) |
| Hohe Raum-Zeit-Ausbeuten | Geringerer Energiebedarf | Geringere Entsorgungskosten |
| Hochspezifische Katalyse | Weniger Abfall-/Nebenprodukte und toxische Substanzen | |
| Hohe Stereo-/Enantioselektivität | Biologische Abbaubarkeit von Katalysator | |
| Verbesserte Umweltbilanz | ||
| Höhere Verfahrenssicherheit |
Die wirtschaftlichen und ökologischen Vorteile biotechnologischer gegenüber konventionellen Produktionsweisen werden am Beispiel der Vitamin-B2-Produktion deutlich. Die Umstellung auf eine biotechnologiebasierte Produktion erbrachte folgende Einsparungen [Schüler, J. (2016), S. 258]:
- Reduktion des Ressourceneinsatzes (Material und Energie) um bis zu 60 %
- Kosteneinsparung in der Produktion bis zu 40 %
- Verringerung des Abfallaufkommens um bis zu 95 %
- Einsparung von CO2 bis zu 30 %
Quelle(n):
- Kagermann, H.; Barner, A. und Hacker, J. und Kreiner, C. (2017): Innovationspotenziale der Biotechnologie, Herbert Utz Verlag, München, acatech IMPULS, ISBN 978-3-8316-4612-8.
- biotechnologie.de c/o BIOCOM AG; Graf, P. und Wirsching, S. (2015): Weiße Biotechnologie - Chancen für eine biobasierte Wirtschaft. Bundesministerium für Bildung und Forschung (BMBF), Berlin [abgerufen am: 07.01.2020], verfügbar unter: Link
- Schüler, J. (2016): Die Biotechnologie-Industrie, Springer Berlin Heidelberg, ISBN 978-3-662-47159-3.
- Braun, M.; Teichert, O. und Zweck, A. (2006): Biokatalyse in der Industriellen Produktion - Fakten und Potenziale zur weißen Biotechnologie. Zukünftige Technologien Consulting der VDI Technologiezentrum GmbH, Düsseldorf [abgerufen am: 19.11.2019], verfügbar unter: Link
Überblick zu Rohstoffen und biobasierten Produkten
Zu den Rohstoffen, die in industriellen biotechnologischen Verfahren verarbeitet werden, zählen Anbaubiomasse, Abfälle und Abgase sowie Sonnenlicht und CO2. Unter der Anbaubiomasse werden Stärkepflanzen, Lignocellulose, grüne (nasse) Rohstoffe (z. B. Gras) und Ölpflanzen verstanden [Schüler, J. (2016), S. 288 ff.].
Ungenutzte und umweltverschmutzende Abfälle, Abgase und Reststoffe aus der Landwirtschaft, der industriellen Produktion oder dem kommunalen Bereich können durch den Einsatz in Verfahren der weißen Biotechnologie recycelt oder veredelt werden [Schüler, J. (2016), S. 288 ff.], [Übelhör, V. und Sameith, J. (2019)].
Zu den typischen Produkten aus biotechnologischen Produktionsverfahren zählen [Schüler, J. (2016), S. 257], [DPWB (2008)]:
- Plattformchemikalien, Wirkstoffe und Biokatalysatoren für die chemische und pharmazeutische Industrie (z. B. Feinchemikalien, Monomer-Bausteine für biobasierte Kunststoffe)
- Zusatzstoffe für Verbrauchsgüter (z. B. Waschmittelenzyme, kosmetische Wirksubstanzen)
- Zusatzstoffe für eine gesunde und umweltschonende Ernährungsweise (z. B. Aminosäuren, natürliche Aromastoffe, Vitamine, Säuerungsmittel, Verdickungsmittel)
- Hochwirksame Enzyme für umweltschonende Prozesse wie der Papier- oder Textilindustrie)
Quelle(n):
- Schüler, J. (2016): Die Biotechnologie-Industrie, Springer Berlin Heidelberg, ISBN 978-3-662-47159-3.
- Übelhör, V. und Sameith, J. (2019): Biobasierte Technologien für die Zukunft – Für eine bessere Nutzung biogener Ressourcen. Hessen Trade & Invest GmbH, Wiesbaden [abgerufen am: 20.12.2019], verfügbar unter: Link
- DPWB (2008): Weiße Biotechnologie – die Erfolgsgeschichte geht weiter. DPWB, heute IWBio – Industrieverbund Weiße Biotechnologie (Nationale Plattform Weiße Biotechnologie), Berlin.
Projekte
BIOBASIERTE ABFALLSTOFFE: PhosFarm – Nachhaltige Phosphorrückgewinnung aus landwirtschaftlichen Reststoffen durch einen enzymatischen Prozess
- Entwicklung eines biotechnologischen Verfahrens zur Rückgewinnung von Phosphor/Phosphaten aus landwirtschaftlichen Reststoffen und Abfällen der Nahrungsmittelindustrie
- Einsatz von Enzymen zur Umwandlung des organisch gebundenen Phosphors in anorganisches Phosphat
- Auswahl der Enzyme bezüglich Selektivität, Spezifität und Verfügbarkeit sowie Optimierung der Hydrolyse hinsichtlich der Reaktionspartner
- Entwicklung einer mobilen Einheit mit hoher Flexibilität zum Einsatz des Verfahrens in bereits bestehenden Betrieben
- Kombination herkömmlichen Düngemittels mit dem gewonnenen Phosphat und somit optimale Anpassung des Düngers an Bedürfnisse verschiedener Pflanzen
BIOBASIERTE ABFALLSTOFFE: TeFuProt – Technofunktionelle Proteine
- Nutzung pflanzlicher Proteine aus Reststoffen der Landwirtschaftsproduktion mit dem Ziel einer höheren Wertschöpfung gegenüber der momentanen Verwendung (thermische Verwertung)
- Modifizierung pflanzlicher Proteine mit technofunktionellen Eigenschaften für technische Anwendungen (etwa Lacke oder Schmierstoffe)
- Nutzbarmachung pflanzlicher Proteine unterschiedlicher Reinheitsgrade in möglichst vielen technischen Anwendungen
- Untersuchung der Verwertbarkeit der Rückstände aus der Proteinextraktion
- Entwicklung von nach Möglichkeit komplett biologisch abbaubaren und biobasierten Bio-Polymer-Compounds
- Entwicklung eines Verfahrens und Überprüfung der Prozessparameter
BIOBASIERTE ABFALLSTOFFE: bioCONNECT – Schlüsseltechnologie zur Erforschung eines integrativen und domänenübergreifenden Konzepts für Bioraffinerien durch die biokatalytische Methanisierung von grünem Wasserstoff und biogenem CO2
- Entwicklung einer innovativen Technologie zur biologischen Methanisierung von „grünem Wasserstoff" und biogenem Kohlendioxid aus Biogasanlagen
- CO2-freier Produktionsprozess für die alkoholische Gärung und Entwicklung einer Pilotanlage
- Steigerung der Effizienz der Bioethanolproduktion durch Verwertung der Schlempe in Biogasanlagen und Verwertung des CO2 aus der Biogasproduktion per Methanisierung
- Nutzung von Wasserstoff aus der Power-to-Gas-Technologie und Erforschen der Speicherung von regenerativem Überschussstrom in Form von Wasserstoff bzw. Methan
BIOBASIERTE ABFALLSTOFFE: CarboSurf – Neue Verfahren zur fermentativen Herstellung von Glykolipid-Biotensiden und sialylierten Kohlenhydraten
- Entwicklung innovativer Fermentationsverfahren zur Herstellung von bestimmten Verbindungen
- Glykolipid-Bio-Tenside: breite Palette von Anwendungsbereichen
- Spezielle Kohlenhydrate: für neutrazeutische, pharmazeutische und kosmetische Inhaltsstoffe - Entwicklung von mikrobiellen Produzentenstämmen durch Metabolic Engineering
- Entwicklung eines industriellen Prozesses durch Optimierung des Fermentationsprozesses und nachfolgende Verarbeitung
- Schwerpunkt auf Identifizierung und Behebung der Engpässe in der Wertschöpfungskette
BIOBASIERTE ABFALLSTOFFE: ChiBio – Entwicklung einer integrierten Bioraffinerie zur Verarbeitung von chitinreichem Abfall zur Herstellung von Spezial- und Feinchemikalien
- Entwicklung von Verfahren zur Verwertung von Fischereiabfällen für die Herstellung von Spezial- und Feinchemikalien
- Erstellen einer Enzym-Toolbox zur Degradation von Chitin in seine Oligo- und Monomere
- Hydrolyse des Chitins mit Chitinasen
- Identifikation von Mikroorganismen mit der Fähigkeit, Chitin als Substrat zu verwenden
- Entwicklung eines Prozesses mit wiederholter Nutzung der chitinolytischen Enzyme, erhöhter Aktivität der Enzyme und garantierter In-situ-Produktabtrennung
- Untersuchung der technischen Machbarkeit der neuen Methoden und Durchführung einer Lebenszyklus- und Kostenanalyse
BIOBASIERTE ABFALLSTOFFE: INDIE – Biotechnological production of sustainable indole
- Entwicklung mikrobieller und biokatalytischer Verfahren zur Herstellung von Indolen (Aromastoff für Molkereiprodukte, Teegetränke und Parfüm)
- Verfahrensentwicklung basiert auf „Entwickeln-Herstellen-Testen-Lernen-Zyklen“ mit dem Bakterium C. glutamicum zur Produktion von Indolen
- Anwendung eines Stoffwechselmodells zur Beschreibung der biochemischen Stoffwechselwege des Bakteriums C. glutamicum zur Ermittlung eines optimalen Produktionsweges bei reduziertem Ressourceneinsatz und geringen Kosten
BIOBASIERTE ABFALLSTOFFE: P4SB – From Plastic waste to Plastic value using Pseudomonas putida Synthetic Biology
- Entwicklung eines Verfahrens zum Kunststoff-Upcycling durch biotechnologische Abfallverwertung
- Einsatz von Enzymen (Esterasen) zum Zerlegen der Kunststoffe in Monomere
- Verwerten der Monomere durch Mikroorganismen (Bakterium: Pseudomonas putida) und Erzeugen komplexerer Kunststoffe
- Vorteil gegenüber chemischen Reaktionen: Verfahren unempfindlich gegenüber Verunreinigungen und Verwertung von bis zu vier verschiedenen Monomeren gleichzeitig durch die Mikroorganismen
CELLULOSE UND LIGNOCELLULOSE: Allianz FuPol – Funktionalisierung von Polymeren
- Nutzbarmachung biobasierter Polymere (Lignin, Cellulose) aufgrund chemischer Aktivierung durch Enzyme
- Funktionalisierung von Lignin
- Lignin ist frei verfügbares, erneuerbares und umweltfreundliches Biopolymer, hat jedoch geringe Wasserlöslichkeit
- Enzymatische Funktionalisierung von Lignin und dadurch erhöhte Wasserlöslichkeit durch die Verwendung von Laccasen
- Enzymatische Modifizierung von Lignin als erneuerbaren Zusatzstoff für Beton
- Einsparung von Energie und Wasser
- Funktionalisierung von Cellulose
- Funktionalisierter natürlicher Biopolymer Cellulose kann als Betonverflüssiger für leichte bis mittlere Wasserreduktion eingesetzt werden
- Löslichkeit von Cellulose eine große Herausforderung
- Entwicklung von maßgeschneiderten Biokatalysatoren für eine umweltfreundliche und kosteneffiziente Modifikation von Cellulose
- Neue Enzyme für Waschmittel
- Entwicklung neuer Waschmittelenzyme für Kunstfasertextilien
- Entwicklung auf Basis von existierenden Enzymen oder zu findenden Wildtyp-Enzymen mittels gelenkter Evolution und rationalen Designs
- Veredelung von Funktionsgarnen
- Entwicklung von Färbe- und Oberflächenveredelungsprozessen für die Textilindustrie
- Identifikation von Peptid-Ankern als biologische Alternative zu herkömmlichen Verfahren mit schädlichen Nebenprodukten bei der Gewinnung von synthetischen Polymeren
CELLULOSE UND LIGNOCELLULOSE: KomBiChemPro – Fein- und Plattformchemikalien aus Holz durch kombinierte chemisch-biotechnologische Prozesse
- Entwicklung eines integrierten Bioraffineriekonzepts zur stofflichen Nutzung von lignocellulosehaltiger Biomasse
- Betrachtung der gesamten Prozesskette der stofflichen Verwertung von Lignocellulose
- Fermentationsentwicklung zur Produktion von Xylonsäure und Äpfelsäure aus den C5-Zuckern der Hemicellulosefraktion
- Experimente im Labor- und Technikumsmaßstab und anschließendes Scale-up in den 10-m³-Maßstab
CELLULOSE UND LIGNOCELLULOSE: Lignocellulose-Bioraffinerie – Aufschluss lignocellulosehaltiger Rohstoffe und vollständige stoffliche Nutzung der Komponenten (Phase 2)
- Entwicklung eines Prozesses zur Gewinnung von biobasierten Produkten auf Cellulose-, Hemicellulose- und Ligninbasis innerhalb einer Bioraffinerie
- Entwicklung, Bau, Inbetriebnahme und Optimierung einer Pilotanlage zum OrganoSolv-Aufschluss von Lignocellulose
- Bereitstellung der Fraktionen aus dem Aufschluss und Weiterverarbeitung zu höherwertigen Produkten
- Entwicklung von Wertschöpfungsketten für die Zuckerfraktionen zum Nachweis der Eignung der aus Aufschluss und Hydrolyse gewonnenen Fraktionen für die gewählten Applikationen
- Testen physikalisch-chemischer und biotechnologischer Verfahren zur Verwendung von Ligninmonomeren als Plattformchemikalien oder Katalysatoren in der Chemischen Industrie
- Identifikation ökonomischer und ökologischer Schlüsselgrößen einer Lignocellulose-Bioraffinerie
CELLULOSE UND LIGNOCELLULOSE: LignoPlast – Funktionalisierte Ligninspaltprodukte als Synthesebausteine für die Herstellung von Klebstoffen, Lacken, Polyurethanen und Epoxiden
- Entwicklung von Verfahren für die Herstellung von Klebstoffen, Lacken und Kunststoffen aus Holz (Lignin)
- Entwicklung innovativer Verfahren zur Herstellung aromatischer Synthesebausteine aus verschiedenen Lignintypen
- Gewinnung der Synthesebausteine durch Abbau der makromolekularen Struktur der Lignine und gezielte chemische und enzymatische Funktionalisierung
- Funktionalisierung von Ligninbruchstücken mittels oxidativer Enzyme
- Erschließung neuer bakterieller Enzyme zur gezielten Modifikation von Ligninderivaten
CELLULOSE UND LIGNOCELLULOSE: WooBAdh – Environmentally-friendly bioadhesives from renewable resources
- Entwicklung eines Verfahrens zur Herstellung von biobasierten Klebstoffen
- Substitution von Formaldehyd durch biobasierte Substanzen, gewonnen aus pflanzlichen oder holzbasierten Stoffen
- Herstellung von biobasierten Klebstoffen durch chemische oder enzymatische Modifizierung von Lingnin oder Tannin
- Vermeidung von Emissionen flüchtiger organischer Substanzen (wie Formaldehyd) beim täglichen Einsatz von Klebstoffen
Demozelle Smarte Fabrik 4.0
- Simulation der Fertigung individueller Produkte in kleinen Stückzahlen durch "digitalen Zwilling" des Produktionsprozesses (digitale Prozesskette vom Produktmodell zum Produktionsprozess)
- Ermöglicht es, die Herstellbarkeit eines Produktes automatisch zu bewerten, den Prozess ggf. anzupassen und den Ressourcenverbrauch der Herstellung vorab abzuschätzen
- Demonstration dieser Vorgehensweise in der "Smart Factory 4.0" anhand eines vereinfachten Produktionsprozesses (Herstellung eines Kaffeeuntersetzers)
NACHWACHSENDE ROHSTOFFE: BayBiotech – Ressourcenschonende Biotechnologie in Bayern
- Bildung eines Projektverbundes bestehend aus bayerischen Forschungsinstitutionen und Unternehmen zur Erforschung und Untersuchung industriell, biotechnologisch hergestellter Produkte:
- Ressourcenschonende Herstellung von Feinchemikalien
- Entwicklung neuer Ganzzellbiokatalysatoren
- Biofilme für die Prozessintensivierung
- Biotechnologische Optimierung der biobasierten Polymerherstellung
- Synthese von Biopolymeren aus Kohlendioxid
- Ressourceneffiziente Produktionsverfahren für PHB-Biokunststoffe
NACHWACHSENDE ROHSTOFFE: Bio-QED – Bio-Quod Erat Demonstrandum: Fermentative Herstellung und Scale-up für die Produktion von 1,4-Butandiol und Itaconsäure mit dem Ziel der Kostenreduktion und ver-besserten Nachhaltigkeit
- Biotechnologische Herstellung von biobasierten Grundchemikalien wie 1,4-Butandiol (BDO) und Itakonsäure (IA) als Alternative zu petrochemischen Quellen
- Erhebung aller technischen und wirtschaftlichen Schlüsselparameter zur Unterstützung bei Investitionsentscheidungen über industrielle Produktionsanlagen für biobasierte Basiskomponenten
- Belegen der technischen, wirtschaftlichen und ökologischen Nachhaltigkeit der Produktion biobasierter Basischemikalien
- Projektablauf:
- Auswahl geeigneter Rohstoffe der 2. Generation und Herstellung von Zuckern
- Toxizitätstest für die mikrobiologische Verwertung
- Etablierung der Fermentation zur Produktion von BDO und IA aus den ausgewählten Rohstoffen
NACHWACHSENDE ROHSTOFFE: BioConSepT – Bioconversion and Separation Technology
- Vollständige energetische und stoffliche Nutzung von biobasierten Rohstoffen der 2. Generation (pflanzliche Öle/Fette und Lignocellulose) zur Herstellung von biobasierten Polymeren
- Bis zu 30 % Kosteneinsparung gegenüber Nutzung von Rohstoffen der 1. Generation
- Entwicklung von Verfahren zur Herstellung von Industriechemikalien aus Bioabfall als Rohstoffquelle
- Entwicklung von Verfahren zur Herstellung von Dicarbonsäuren und Epoxiden aus Pflanzenölen
NACHWACHSENDE ROHSTOFFE: ChitoTex – Entwicklung und Produktion neuer Insektenchitosane und chitosanbasierter funktioneller Beschichtungen für Garne und Textilien
- Insektenchitin als nachhaltige Chitinquelle hinsichtlich funktioneller Oberflächenbeschichtungen für Garne und Textilien
- Nutzung der hoch chitinanteiligen Nebenprodukte aus der insektenbasierten Proteinherstellung
- Identifikation von Reststoffströmen mit Chitingehalt von min 30 % basierend auf eigens dafür entwickelten Analyseverfahren
- Reine biotechnologische Wertschöpfungskette zur Chitinherstellung
- Lokale Alternative zu krabbenbasiertem Chitosan
- Initiierung eines Nachfolgeprojektes zur Anwendung von hydrophobisiertem Chitosan
NACHWACHSENDE ROHSTOFFE: Weiße Biotechnologie mit Pflanzenzellen: Transfer innovativer Verfahren zur Applikation von Pflanzenzellen in die Lebensmittel-, Holz-, Pharma- und Kosmetikindustrie durch eine interdisziplinäre Nachwuchsforschergruppe
- Entwicklung innovativer Verfahren zur Anwendung von Pflanzenzellen in der Lebensmittel-, Holz-, Pharma- und Kosmetikindustrie
- Analyse und Optimierung der Sekundärmetabolit-Produktivität verschiedener transformierter und nicht transformierter Zellen
- Hemmnisanalyse zum Transfer biotechnologischer Verfahren in die industrielle Großanwendung
- Untersuchung von Wirtschaftlichkeit und Umweltauswirkungen ausgewählter Verfahren der weißen Biotechnologie
NACHWACHSENDE ROHSTOFFE: Weiße Biotechnologie zur Wasserstoffsynthese: Entwicklung von Verfahrensgrundlagen zur Gewinnung biogenen Wasserstoffes in neuartigen Photobioreaktoren durch eine interdisziplinäre Nachwuchsforschergruppe
- Umwandlung von Wasserstoff in Energie ist CO2-neutral, jedoch basiert die Wasserstoffherstellung größtenteils auf fossilen Brennstoffen
- Entwicklung eines Verfahrens zur fossilfreien Herstellung von Wasserstoff
- Verfahren: Umwandlung von Sonnenenergie in Wasserstoff mit Hilfe von Biokatalysatoren
- Elektrizität, die in den Brennstoffzellen elektromobiler Fahrzeuge umgewandelt wird, oder Wärme könnte damit klimaschonend produziert werden
Optimierte Methanolsynthese
- Entwicklung einer innovativen und klimafreundlichen Prozesskette zur Synthese der Basischemikalie Methanol
- Kopplung eines Biomasse-Umwandlungsprozesses mit einer Dampfreformierung
- Projektierung eines Druckwechselabsorptionsverfahrens mit ionischen Flüssigkeiten und Prozesskettenevaluation für zwei Modellstandorte
- Bei auf 6 MW Druckfermentation basierender Methanolsynthese von Betriebsbedingungen abhängige negative CO2-Bilanz
PFLANZLICHE ÖLE: Integrierte Bioproduktion – Integrierte chemisch-biotechnologische Herstellung von Synthesebausteinen auf Basis nachwachsender Rohstoffe in einer Bioraffinerie
- Untersuchung biotechnologischer Konversionsverfahren
- Optimierung und Scale-up der fermentativen Herstellung von Plattformchemikalien (Synthesebausteinen) und Biotensiden in den Produktionsmaßstab
- Auswahl geeigneter Katalysatoren im Labormaßstab anhand von relevanten Pflanzenölen
- Anwendungstechnische Untersuchung der Synthesebausteine in unterschiedlichen Produktgruppen
PFLANZLICHE ÖLE: Bioschmierstoffe für Schiffsantriebe
- Entwicklung von Verfahren zur Herstellung von biologisch abbaubaren, hydrolysebeständigen Schmierstoffen aus nachwachsenden Rohstoffen für umweltsensible Anwendungen (z. B. Schmierstoffe für Antriebswellen in Schiffen)
- Entwicklung und Skalierung entsprechender Herstellungsverfahren
- Analyse, Test und Bewertung der neuen Schmierstoffe
- Entwickelte neuartige Schmierstoffe weisen eine erhöhte Stabilität auf und führen zu einer Verlängerung der Ölwechsel-Intervalle
- Einsatz nachwachsender Rohstoffe reduziert den Bedarf an petrochemische Rostoffen
PFLANZLICHE ÖLE: BioSurf – Neue Produktionsstrategie für Biotenside
- Entwicklung neuer kosteneffizienter Verfahren für die mikrobielle und enzymatische Herstellung von Biotensiden
- Biokompatibilität, biologische Abbaubarkeit und geringe Toxizität von Biotensiden im Vergleich zu herkömmlich hergestellten Tensiden
- Entwickeln von Enzymen für die biotechnische Synthese von Tensiden
- Selektieren und Optimieren von Mikroorganismen mit molekularbiologischen Methoden
- Optimieren der Tensidwirkung der neuen Biotenside
- Optimierte Fermentation für Glykolipide
- Durchführung von enzymatischer Optimierung und Metabolic Engineering
- Herstellung von Biotensidvarianten für Anwendungstests
PFLANZLICHE ÖLE: SUSBIND – Entwicklung und Herstellung von nachhaltigen Biobindemitteln für Holzwerkstoffplatten
- Herstellung von biobasierten Bindemitteln für die Produktion von Holzwerkstoffplatten (P2-Spanplatten und mitteldichten Faserplatten)
- Ersetzen von fossilen durch nachwachsende Rohstoffe
- Etablierung und Scale-up von technischen Enzymprozessen
- Nutzung von Nebenprodukten aus bestehenden europäischen Bioraffinerien für Herstellung von Bindemitteln
- Erhöhung der Marktfähigkeit von ausschließlich biobasierten Möbelprodukten
- Verbesserung des Carbon Footprint
- Reduzierung der Treibhausgasemission
- Minimierung der Abhängigkeit von fossilen Rohstoffen
- „Grüner“ Wettbewerbsvorteil gegenüber billigeren, importierten Produkten
Bereitstellung von Biokatalysatoren
Gute Praxis
Automatisierte Entwicklung neuer Produktionsorganismen
Die Entwicklung und Testung von neuen Enzymen und Produktionsorganismen für industrielle biotechnologische Produktionsverfahren erfolgt heutzutage mithilfe automatisierter Prozesse. Dadurch können hohe Durchsatzmengen erzielt werden (Hochdurchsatzverfahren) [Wiechert, W. et al. (2018), S. 6].
Quelle(n):
- Wiechert, W.; Scheper, T. und Weuster-Botz, D. (2018): Neue Schubkraft für die Biotechnologie – Miniaturisierung, Automatisierung und Digitalisierung revolutionieren die Entwicklung biotechnologischer Prozesse und Produkte. DECHEMA Gesellschaft für Chemische Technik und Biotechnologie e.V., Frankfurt am Main [abgerufen am: 12.12.2019], verfügbar unter: Link
Einsatz effektiver Biokatalysatoren
Biokatalysatoren erhöhen die Effektivität und mindern den Energiebedarf einer biochemischen Umsetzung im Reaktor. Um den Mengenverbrauch und die Abfallentstehung an Biokatalysatoren auf ein Minimum zu beschränken, sind bestimmte Aspekte bei dem Einsatz von Biokatalysatoren in einem Reaktionssystem zu berücksichtigen. Verwendete Biokatalysatoren sollten folgende Eigenschaften aufweisen:
- Hohe Katalysatoraktivität
- Hohe Langzeitstabilität
- Geringe Deaktivierungsrate
- Hohe Produkt-Selektivität
Einsatz von Enzymen in der stofflichen Produktion
In der Regel weisen Enzyme (Biokatalysatoren) gegenüber konventionellen Katalysatoren einige entscheidende Vorteile auf [Schiller, J. et al. (2016), S. 42 f.]:
- Hohe Reaktionsselektivität
- Höhere Reaktionsgeschwindigkeit
- Größere Reaktionseffizienz
- Bessere Produktreinheit
- Einen geringeren Energieverbrauch (die Reaktionen finden in der Regel bei Normaltemperatur und -druck statt)
- Geringere Abfallproduktion
- Hohe Aktivität in umweltfreundlichen Lösungsmitteln wie Wasser, Ethanol oder überkritischem CO2
Insbesondere bei der Produktion von chiralen Molekülen erweist sich der Einsatz von Enzymen als Katalysatoren als besonders günstig, denn in vielen Fällen besitzen Enzyme die Eigenschaft der Chiral-Spezifität, d. h., von zwei möglichen chiralen Molekülformen wird nur eine begünstigt. Dies führt in der Regel zu einer Verringerung des Trennungsaufwands [Schiller, J. et al. (2016), S. 42 f.].
Quelle(n):
- Schiller, J.; Aicher, C.; Feresin, E.; Klauer, B. und Hansjürgens, Bernd und Sauter, Arnold (2016): Weiße Biotechnologie - Stand und Perspektiven der industriellen Biotechnologie: Umwelt- und Nachhaltigkeitspotenziale. Innovationsanalyse Teil II. Büro für Technikfolgen-Abschätzung beim Deutschen Bundestag (TAB), Berlin, TAB-Arbeitsbericht 169.
Einsatz von immobilisierten Enzymen
Folgende Vorteile immobilisierter Enzyme sind bekannt [Braun, M. et al. (2006), S. 21 f.], [Castiglione, K. und Weuster-Botz, D. (2018)]:
- Höhere Lebensdauer
- Mehrfacher Einsatz der verwendeten Biokatalysatoren, dadurch Kostenreduktion
- Ermöglichung einer kontinuierlichen Reaktionsführung (Verweilzeitentkopplung)
- Vereinfachte Produktaufreinigung
- Erzielung besserer Produktqualitäten
Nachteilig wirkt sich bei einer Immobilisierung von Enzymen die Verringerung der Reaktionsgeschwindigkeit aus. Dies kann z. B. durch Aktivitätsverluste aufgrund der Enzymfixierung auf dem Feststoff oder durch eine Verringerung der Diffusionsgeschwindigkeit von Reaktanten und Produkten hervorgerufen werden. Der Nachteil einer herabgesetzten Reaktionsgeschwindigkeit kann durch eine mögliche längere Lebensdauer fixierter Enzyme wieder kompensiert werden [Braun, M. et al. (2006), S. 22]. Allerdings fallen durch den Immobilisierungsprozess auch zusätzliche Kosten an, z. B. für Material- und Arbeitsaufwand. Darüber hinaus können immobilisierte Enzyme nur bei gelöst vorliegenden Substraten eingesetzt werden [Castiglione, K. und Weuster-Botz, D. (2018), S. 406].
Die Entscheidung, ob die Verwendung eines immobilisierten oder gelösten Enzyms günstiger ist, muss im Einzelfall getroffen werden. Dazu müssen die im jeweiligen prozessspezifischen Anwendungsfall auftretenden Vor- und Nachteile gegeneinander abgewogen werden.
Quelle(n):
- Braun, M.; Teichert, O. und Zweck, A. (2006): Biokatalyse in der Industriellen Produktion - Fakten und Potenziale zur weißen Biotechnologie. Zukünftige Technologien Consulting der VDI Technologiezentrum GmbH, Düsseldorf [abgerufen am: 19.11.2019], verfügbar unter: Link
- Castiglione, K. und Weuster-Botz, D. (2018): Enzymatische Prozesse. In: Chmiel, H. und Takors, R. und Weuster-Botz, D., Hg. Bioprozesstechnik. 4. Auflage. Springer Berlin Heidelberg, Berlin, S. 403-447, ISBN 978-3-662-54041-1.
Screening- und Analysemethoden
Um einen ressourceneffizienten und wirtschaftlichen biotechnologischen Produktionsprozess umzusetzen, sind die Identifizierung und Bereitstellung geeigneter Enzyme und Mikroorganismen eine wichtige Voraussetzung. Mit Hilfe von Screening- und Analysemethoden können geeignete Enzyme und Mikroorganismen identifiziert werden [Fraunhofer IGB, IME, IAP, ICT, IPA, UMSICHT, IVV, WKI (kein Datum), S. 8 f.].
An einen Prozess angepasste Biokatalysatoren (Enzyme) und Mikroorganismen ermöglichen neben einer kostengünstigeren Produktionsweise einen geringeren Zeitbedarf bei der Entwicklung und Etablierung neuer industrieller biotechnischer Verfahren bzw. Produkte [Schüler, J. (2016), S. 258].
Quelle(n):
- Fraunhofer IGB, IME, IAP, ICT, IPA, UMSICHT, IVV, WKI (kein Datum): Vom Rohstoff zum Produkt – Industrielle Biotechnologie in der Fraunhofer-Gesellschaft. Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. [abgerufen am: 19.11.2019], verfügbar unter: Link
- Schüler, J. (2016): Die Biotechnologie-Industrie, Springer Berlin Heidelberg, ISBN 978-3-662-47159-3.
Projekte
Bakterien recyceln Platingruppenmetalle und produzieren Umweltkatalysatoren zur Entfernung von langlebigen organischen Schadstoffen
- Entwicklung von (bio-)metallurgischen Methoden für die nachhaltige Rückgewinnung von Edelmetallen
- Verwendung von Schwermetall-toleranten Bakterien als Produzenten von hochaktiven Nanokatalysatoren in Form von Edelmetall-Nanopartikeln
- Simultaner Ablauf des mikrobiellen Wachstums, der Metallreduktion und der Nanopartikel-Bildung durch biotechnologischen Prozess
Bi-Amin – Amine nachhaltig produziert
- Entwicklung eines biotechnologischen Verfahrens mit neuen Reaktionsrouten und Katalysatoren zur nachhaltigen Produktion von Aminen
- Verbesserung der Energiebilanz des konventionell bei hohem Druck und hohen Temperaturen ablaufenden Prozesses durch den Einsatz von Enzymen
- Herstellung der Amine nach dem Konzept der zellfreien Biosynthese: Einsatz aufgereinigter, spezifischer Enzyme, die zu rein enzymatischen Reaktionskaskaden zusammengesetzt werden
Biokonversion von Fettsäuren heimischer Ölpflanzen zu bioaktiven Naturstoffen für Lebensmittel-, Kosmetik- und Pharmaindustrie
- Entdeckung von ruhenden Hefezellen als Biokatalysator zur Synthese von Grünnoten (aldehyd-basierten Aromastoffen im Lebensmittelbereich)
- Biokatalytisches Verfahren als effiziente Alternative zum konventionellen Verfahren
- Untersuchung verschiedener Verfahren zur Gewinnung der Aldehyde aus dem Produktgemisch (Produkt, Edukt, Biokatalysator)
- Aussichtsreichstes Verfahren zur Produktgewinnung: Ausstrippen der flüchtigen Aldehyde und die Adsorption an hydrophobe Harze mit anschließender ethanolischer Extraktion
Boosting Lignocellulose Biomass Deconstruction with Designer Cellulosomes for Industrial Applications
- Erzeugen von Mehrwertchemikalien (z. B. fortschrittliche Biokraftstoffe) durch Aufschlüsseln von Biomasseabfall
- Umwandlung der Zellulose aus den Zellwänden in fermentierbare Zucker
- Senken der Verfahrenskosten und der Menge an Ausgangsmaterialien durch Verzuckerung der Biomasse
- Gewinnung von fermentierbaren Zuckern aus dem organischen Anteil von Siedlungsabfällen durch die Entwicklung von Designer-Zellulosomen aus natürlichen Zellulosomen und lignozellulosehaltigen Enzymen
- Untersuchen der physiochemischen, atomischen und supramolekularen Struktur des Zellulosoms
- Charakterisierung der zellulosomalen und nichtzellulosomalen Komponenten in einem standardisierten Enzym-Assay
Cellulect – A Synthetic Biology Platform for the Optimization of Enzymatic Biomass Processing
- Biomasse in Zucker durch „Frontend“ umwandeln und anschließend zur Herstellung nützlicher Produkte weiterverwenden
- Schnelle Abstimmung eines Bakteriums oder Pilzes, um eine optimale Biomasse-Umwandlung zu ermöglichen
- Technologie überall in Bioraffinerien verbindbar
Entwicklung und Herstellung mechanisch stabiler Enzympräparate zur biokatalytischen Synthese von Spezialchemikalien aus nachwachsenden Rohstoffen Teilvorhaben 2: Immobilisatenentwicklung und Verfahrensoptimierung
- Entwicklung neuartiger Biokatalysatorsysteme zur nachhaltigen Synthese von Spezialchemikalien auf Basis nachwachsender Rohstoffe
- Einsatz adsorbierter Enzyme auf Trägermaterialien
- Adsorbierte Enzyme zeigen hohe Stabilitäten gegenüber mechanischen Kräften sowie gegenüber Proteindesorption im Herstellungsprozess: Möglichkeit einer hohen Wiederverwendbarkeit gegeben
HOMBIOCAT – Fabrication of hierarchically organized multifunctional heterogeneous biocatalysts for the modular synthesis of ω-amino acids from renewable feedstocks
- Entwicklung einer Toolbox zur Herstellung effizienter, multifunktionaler Biokatalysatoren
- Einsatz der multifunktionalen Biokatalysatoren zur Herstellung von Produkten aus nachwachsenden Rohstoffen
- Zur Herstellung der multifunktionalen Biokatalysatoren werden Multi-Enzymsysteme im nano-skaligen Bereich auf festen und porösen Materialien mit Hilfe von Protein-„Arbeitsplattformen“ aufgebaut
- Die auf festen Materialien adsorbierten Enzyme sind hierarchisch und räumlich organisiert
HyPerIn – Integrative Approach to Promote Hydroxylations with Novel P450 Enzymes for Industrial Processes
- P450-Enzyme gelten in der organischen Chemie als „potenziell die nützlichste aller Biotransformationen“
- Anwendung wird in der Industrie durch technische Engpässe erschwert
- Aufbau einer Plattform für die Identifizierung und Optimierung neuer rekombinanter P450-Expressionssysteme
- Schwerpunkt liegt auf Integration von mikroskaligen Hochdurchsatz-Prozessentwicklungsmethoden mit der Biokatalyse-Entwicklung
Innozym – Effiziente Herstellung industrierelevanter Enzyme
- Entwicklung effizienter, rekombinanter Expressionsverfahren zur Produktion technischer Enzyme sowie Herstellung und Aufreinigung bis zu einem Maßstab von 10 m3
- Entwicklung geeigneter Produktionsstämme und Optimierung der Bioprozesstechnik
- Evaluierung pro- und eukaryotischer Expressionsstämme sowie Entwicklung von Vektoren für die Produktion industriell relevanter Hydrolasen und Oxidoreduktasen
- Verfahrensentwicklung und -optimierung bis in den Pilotmaßstab für ausbeutereichste Varianten aus dem Labormaßstab
Light-driven sustainable biocatalysis training network
- Nutzung von Cyanobakterien als Biokatalysatoren für lichtgetriebene biotechnologische Anwendungen im Rahmen von industriell relevanten Modellreaktionen
- Ersetzen teurer Reduktionsäquivalente zum Einschleusung der Enzyme in Cyanobakterien und somit Kopplung an die Photosynthese der Bakterien
- Erreichen des Wegfalls teurer Abfall- und Nebenprodukte sowie einer schnelleren, leichteren und kostengünstigeren Herstellung von Chemikalien
- Übertragen der Erkenntnisse aus dem Labor auf Prozesse im industriellen Maßstab
- Erhöhung der Effizienz, mit der Lichtenergie geerntet und an enzymatische Reaktionen weitergegeben werden kann
MetaCat – A metagenomic collection of novel and highly efficient biocatalysts for industrial biotechnology
- Erstellung einer MetaCat-Enzym-Sammlung: innovative Werkzeugsammlung und Erkenntnisse für die Identifizierung von robusten „Allround-frequent-hit“-Enzymen (AFHs)
- Innovationspool für den Nachweis von Enzymen: innovative zellfreie und einzellige Werkzeuge für den funktionalen Metagenom- und Genomabbau
- Enzymanwendungen senken den Einsatz von hochtoxischen konventionellen Katalysatoren deutlich und reduzieren die Umweltbelastung
- Biokatalytische Prozesse senken Energieverbrauch und ‑kosten, da sie bei milderen Prozessbedingungen durchgeführt werden können
ZeroCarbFP – Funktionale Biomasse aus kohlenstoffreichen Abfallströmen
- Erzeugung funktionaler Biomasse aus kohlenstoffreichen Abfallströmen für eine nachhaltige, biologische Synthese von Wertstoffen
- Bei der Herstellung von Biodiesel fallen große Mengen von Rohglycerin als Nebenstrom an
- Entwicklung optimierter Produktionsstämme, welche Rohglycerin effizient nutzen können
- Neue und wertvolle aus Glycerin generierte Produkte können die Wirtschaftlichkeit der Biodieselproduktion deutlich verbessern
- Entwicklung von neuen Verfahren zur vollständigen Verwertung der für die Biodieselproduktion eingesetzten Fette/Öle in einem Bioraffineriekonzept
Prozessmodellierung & -simulation
Gute Praxis
Modellierung von Bioprozessen
Mit Hilfe mathematischer Modelle kann ein Bioprozess beschrieben werden. Bei der Verfahrensentwicklung und Verfahrensoptimierung können validierte mathematische Modelle dabei unterstützen, die Material- und Energieeffizienzpotenziale eines Bioprozesses auszuschöpfen. Modelle unterstützen bei der Auswahl der am besten geeigneten Technikkombinationen unter verschiedenen möglichen Kombinationen im Rahmen der Verfahrensentwicklung. Und sie können den Verfahrensentwicklungsweg von der Labor-, Technikums- und Produktionsanlage im Industriemaßstab beschleunigen, mit dem Ergebnis, dass weniger Material- und Energieaufwände anfallen. Umsatzsteigerungen können im Rahmen von Verfahrensoptimierungen durch die Anwendung mathematischer Modellbeschreibungen herangezogen werden [Fraunhofer IGB, IME, IAP, ICT, IPA, UMSICHT, IVV, WKI (kein Datum), S. 11].
Bei herkömmlichen chemischen Prozessen ist die Verfahrensbeschreibung anhand von (modularen) Modellen in der Praxis angekommen. Die Systembeschreibung von Bioprozessen ist allerdings noch nicht so weit verbreitet. Dies liegt an der hohen Komplexität der Bioprozesse. Eine mathematische Abbildung biotechnologischer Prozesse ist daher um einiges komplizierter, verglichen mit herkömmlichen chemischen Verfahren. Hier besteht noch Forschungs- und Entwicklungsbedarf, der sich aufgrund der Nützlichkeit mathematischer Prozessbeschreibungsmodelle sicherlich lohnt [Fraunhofer IGB, IME, IAP, ICT, IPA, UMSICHT, IVV, WKI (kein Datum), S. 11].
Quelle(n):
- Fraunhofer IGB, IME, IAP, ICT, IPA, UMSICHT, IVV, WKI (kein Datum): Vom Rohstoff zum Produkt – Industrielle Biotechnologie in der Fraunhofer-Gesellschaft. Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. [abgerufen am: 19.11.2019], verfügbar unter: Link
Projekte
ComRaDes – Computation for Rational Design: From Lab to Production with Success
- Beschleunigung der Bioprozessentwicklung inclusive Anlagenentwicklung und -bau um bis zu 20 %
- Entwicklung und Demonstration eines rechnerischen Rahmens (Modell und Simulation) für das rationale Design robuster mikrobieller Stämme und schnell skalierbarer Bioprozesse
- Reduzierung der bisher benötigten Energiemenge und damit einhergehenden CO2-Emissionen um 10 – 30 %
Entwicklung eines Rapid-Prototyping-Ansatzes zum schnellen und effizienten Aufbau optimaler Prozessführungsstrategien für biotechnologische Produktionsprozesse
- Entwicklung eines automatischen Modellgenerators
- Umsetzung von Ideen zur automatischen Struktursuche und dynamischen Anpassung von Modellen
- Erzeugung einer Vielzahl von unterschiedlichen Modellkandidaten erleichtert die Prozessmodellierung und führt zu einer ressourcensparenden Prozessführung
Modellgestützte Optimierung von Platten-Photobioreaktoren (PBR)
- Modellgestützte Optimierung der Kultivierung von phototrophen Einzellern und pflanzlichen Gewebekulturen unter Berücksichtigung von Reaktorgeometrie und Prozessführung
- Entwicklung eines mathematischen Modells
- Berechnung von Wachstumsverhalten von phototrophen Mikroorganismen in Abhängigkeit des Lichteintrags und der Strömungsführung mittels des mathematischen Modells effektiv möglich
- Verbesserung realer Kultivierungssysteme durch Simulation und Parametervariation basierend auf dem mathematischen Modell
ScaleApp – Investigating large scale bioreactor effects in microbial application
- Entwicklung von Scale-down-Verfahren (Modelle) von Bioreaktoren
- Kombination von leistungsstarker CFD (Computational Fluid Dynamics) und innovativer Prozessanalytik
- Erreichung von Verbesserungen in der Bioprozessentwicklung durch erhöhten Informationsgewinn auf Laborebene (verbesserte Entscheidungsbasis)
- Geringere Enzwicklungszeiten und höhere Prozesssicherheiten
Prozessentwicklung & -automatisierung
Gute Praxis
Advanced Process Control Methoden
Bei komplexen Prozessen ist es nicht trivial, den Prozessverlauf möglichst nah an das energetische Optimum hinzuführen. In solchen Fällen sorgen Advanced Process Control (APC) Methoden für einen optimierten Betrieb der eingesetzten Regler. Die in den APC-Methoden angewendeten Prozesskenntnisse werden aus Prozessmodellen und Erfahrungswissen (z. B. Störgrößenaufschaltung) gewonnen. Der Aufwand einer Implementierung und Anwendung der APC-Methoden war bisher recht hoch, dem Einsatz entsprechend erst bei sehr hohen Komplexitätsgraden (z. B. großen Kontianlagen) sinnvoll. Mittlerweile sind jedoch auch Standard-Softwaremodule für Prozessleitsysteme verfügbar, die den Einsatz bei kleineren Anwendungen (kleine Konti- oder Batchanlagen) interessant machen. Die Komplexitätsgrenzen, bei denen sich ein Einsatz lohnt, wurden deutlich herabgesenkt.
Folgende gängige Methoden stehen zur Auswahl und sind für Konti- und Batchanlagen geeignet:
- Statistikbasierte APC-Methode (datengetriebene Methoden): Bei dieser Methode basiert die Ermittlung einer optimierten Stellgröße auf der statistischen Auswertung des zeitlichen Verlaufs von Prozessgrößen und dem daraus gewonnenen statistischen Prozessmodell. Vor der Übergabe der ermittelten Stellgröße an den Regler wird diese mit den Erfahrungswerten des Anlagenbedieners abgeglichen und gegebenenfalls angepasst.
- Modellgestützte prädikative Regelung (MPC): Bei dieser Methode wird durch die Entwicklung und Anwendung eines dynamischen Modells für das betrachtete Verfahren das zukünftige Prozessverhalten (Verlauf von Prozessgrößen) vorhergesagt. Dies erlaubt ein gezieltes Optimieren der Stelleingriffe an der Basisregelung. Ziel dabei ist es, den optimalen Betriebspunkt zu erreichen.
- Online-Optimierung: Diese Methode basiert auf der Anwendung stationärer, rigoroser Modelle. In Abhängigkeit der vorliegenden Prozesszustandsgrößen berechnet ein Online-Optimierer den optimalen Arbeitspunkt für eine energetisch und stofflich effiziente Betriebsweise. Als Ergebnis der Online-Optimierung werden Sollwerte für die untergeordnete Basisregelung ermittelt. Optimierungskriterium kann beispielsweise eine Kostenfunktion aus Rohstoff- oder Energiekosten sein.
Praxisbeispiel(e) finden Sie unter www.namur.net/uploads/tx_press/atp_02_2008_Prozessfuehrung.pdf (S. 71 – 75).
Quelle(n):
- Hagenmeyer, V. und Piechottka, U. (2009): Innovative Prozessführung – Erfahrung und Perspektiven. atp edition, Heft 1-2 S. 53, 57 ff.
- NAMUR, Arbeitskreis 4.17 „Energieeffizienz“ (2012): Vorgehensweise zur Steigerung der Energieeffizienz in chemischen Anlagen – Beitrag der Automatisierungstechnik. Arbeitsblatt NA 140., NAMUR S. 8
Elektrische Leitfähigkeit
Die Ermittlung der Ionenkonzentration in wässrigen Lösungen erfolgt durch Messung der Leitfähigkeit. Die Kenntnis der Ionenkonzentration dient z. B. zur Qualitätsbestimmung von Abwässern, zur Gehaltsbestimmung von Säuren, Laugen und Galvanik-Bädern oder zur Überwachung von Ionentauscheranlagen. Leitfähigkeitsmessgeräte bestehen aus einem Messfühler und einer Auswerte- und Anzeigeeinheit. Für die Messung niedriger und hoher Ionenkonzentrationen besteht der Messfühler aus zwei konzentrisch angeordneten Elektroden. Der Messfühler wird direkt in die wässrige Lösung eingetaucht und dabei an einer Rohrleitung oder einem Behälter befestigt (angeflanscht). Das Messgerät ist empfindlich durch Partikel verursachte Verschmutzungen und muss in regelmäßigen Abständen kalibriert werden.
Quelle(n):
- Ignatowitz, E. (2013): Chemietechnik. 11. Auflage, Verlag Europa-Lehrmittel, Haan-Gruiten. S. 283
Ex-situ-Sensoren
Ex-situ-Sensoren kommen immer dann zum Einsatz, wenn entweder die Reaktionsbedingungen im Bioreaktor für einen In-situ-Sensor zu widrig sind (z. B. Fouling) oder aber wenn für den zu bestimmenden Messparameter keine In-situ-Sensoren existieren. Bei Ex-situ-Sensoren erfolgt die Messung außerhalb des Reaktors. Dabei kann die Messwertaufnahme kontinuierlich oder diskontinuierlich in bestimmten Zeitintervallen stattfinden. In beiden Fällen werden die Messdaten mit einer zeitlichen Verzögerung, bedingt durch den Probenahmeprozess, aufgenommen. Bei einem dynamischen Bioprozess (z. B. Kultivierungs- oder Aufarbeitungsprozess) führen eine zeitliche Verzögerung der Messwertaufnahme und/oder größere Analyseintervalle zu Informationsverlusten. Existieren Modellbeschreibungen der betreffenden Prozesse, so können die Informationsverluste kompensiert werden. Handelt es sich um nicht so dynamische Prozesse, spielen die zeitlichen Verzögerungen bei Ex-situ-Sensoren keine große Rolle. Prinzipiell sollten Sensoren zum Einsatz kommen, die über ein kurzes und konstantes Ansprechverhalten verfügen [Hitzmann, B. und Scheper, T. (2018), S. 265].
Quelle(n):
- Hitzmann, B. und Scheper, T. (2018): Bioprozessanalytik und -steuerung. In: Chmiel, H. und Takors, R. und Weuster-Botz, D., Hg. Bioprozesstechnik. 4. Auflage. Springer Berlin Heidelberg, Berlin, S. 263-297, ISBN 978-3-662-54041-1.
In-situ-Sensoren
In-situ-Sensoren sind im Reaktor fest eingebaut und liefern in bestimmten Zeitabständen kontinuierlich Messdaten. Die Vorgänge im Reaktor und das Reaktorverhalten insgesamt können somit abgebildet werden. Allerdings gibt es bei biotechnologischen Einsätzen von In-situ-Sensoren eine Besonderheit: In den meisten Fällen findet die Reaktion in einer sterilen Umgebung statt. Der In-situ-Sensor kann nur vor dem Einbau in das „sterile“ Reaktorsystem kalibriert werden. Um die sterilen Bedingungen im Reaktor nicht zu gefährden, ist eine Kalibrierung während des Bioprozesses nicht möglich. Treten allerdings während des Einsatzes eine Sensoralterung oder Fouling-Prozesse im Reaktor auf, dann ändert sich das Ansprechverhalten des Sensors und eine Kalibrierung wäre notwendig, um korrekte Messwerte die Qualität und Quantität betreffend zu liefern. Idealerweise kompensieren die In-situ-Sensoren ein sich änderndes Ansprechverhalten selbstständig. Die Anforderungen an einen In-situ-Sensor sind dementsprechend hoch [Hitzmann, B. und Scheper, T. (2018), S. 265].
Quelle(n):
- Hitzmann, B. und Scheper, T. (2018): Bioprozessanalytik und -steuerung. In: Chmiel, H. und Takors, R. und Weuster-Botz, D., Hg. Bioprozesstechnik. 4. Auflage. Springer Berlin Heidelberg, Berlin, S. 263-297, ISBN 978-3-662-54041-1.
Konzentration (Inline-Messung)
Bei der Anwendung von Inline-Konzentrationsmessverfahren ist eine aufwendige Probenaufbereitung nicht mehr notwendig. Die Verwendung von Laborchemikalien und ‑geräten sowie die Inanspruchnahme zusätzlicher Räumlichkeiten entfallen dementsprechend. In der Regel beeinflussen Inline-Messverfahren das Messmedium in geringerem Maße, verglichen mit Offline-Verfahren. Dies führt zu genaueren Messungen sowie kürzeren Messtotzeiten und damit zu einer besseren Ausregelung, sprich effektiveren Nutzung der Anlage. Zudem erlauben die deutlich verkürzten Messzeiten ein schnelleres Erkennen und Vermeiden von unzulässigen Anlagenzuständen.
Gängige Inline-Messverfahren:
- ATR-Spektroskopie (MIR-Bereich): ATR-Spektroskopie ist vor allem für Gase geeignet, jedoch auch für Flüssigkeiten. Als Lichtwellenleiter kommen die Materialien Halegonid und Chalkogenid in Frage (Quarz nicht). Vorteil ist in dem Fall, dass die Verwendung optischer Multiplexer und damit eine simultane Messung an verschiedenen Stellen möglich ist. Die Materialien weisen jedoch schlechte mechanische Eigenschaften auf. Alternativ wird ein Hohlleiter-Spiegelsystem verwendet, das die Strahlung auf den ATR-Kristall lenkt. Die Sonden sind Kombinationen auf einem IR-durchlässigen Kristall, gepaart mit der eigentlichen ATR-Schicht aus – je nach Wellenlänge – Diamant, Silizium, Zirkonium. Solche Systeme sind bis 100 bar und 250 °C einsetzbar.
- Laser-Spektroskopie: Bei der Laser-Spektroskopie wird der Laserstrahl direkt durch die zwei Fenster in der Rohrleitung vom Sender zum Empfänger geschickt. Es können lediglich Gase, diese aber unabhängig von der Temperatur des Mediums, vermessen werden. Mit Diodenlaser-Spektrometern können nur kleinere Moleküle erfasst werden. Einer der wichtigsten Anwendungsfälle ist hier die Sauerstoffbestimmung mittels AlGaAs-Lasern. Mit InGaAs-Lasern lassen sich eine Reihe weiterer kleiner Moleküle bestimmen (CO, HCl, HCN, NO etc.). Der Trend bei dieser Technologie geht zu Quantenkaskadenlasern. Mit dieser Technik konnte die Messempfindlichkeit erheblich gesteigert und das Spektrum an messbaren Substanzen signifikant erhöht werden. Die „Fenster-Technologie“ wurde in den letzten Jahren deutlich verbessert, so dass sich die Messfehler deutlich verringert haben. Mittels spezieller Fensterflansche ist es heute möglich, Messstörungen zu vermeiden, Verschmutzungen vorzubeugen und eine Reinigung mit Dampf zu ermöglichen.
- NIR-Spektroskopie: Das Anwendungsspektrum der NIR-Spektroskopie konnte sich in den letzten Jahrzehnten insbesondere durch komplexe chemometrische Auswertealgorithmen von einem Online-Verfahren zu einer Inline-Methode entwickeln. Der Aufbau umfasst eine optische Sonde, Lichtwellenleiter und das Spektrometer selbst. Die rechnergestützte Auswertung macht es nach Ermittlung geeigneter Kalibrierungen möglich, komplexe flüssige Stoffgemische in ihrer Konzentration, aber auch in Bezug auf Temperatur, Dichte, Viskosität oder Säurezahl zu überwachen. Entsprechend breit gefächert ist der Anwendungsbereich: Produkteingangskontrolle, Verfahrensüberwachung, Qualitätssicherung, aber auch Reaktionsaufklärung sind möglich. Die simultane Überwachung mehrerer Messstellen mit einem Spektrometer ist ebenso umsetzbar.
- Raman-Spektroskopie: Die Raman-Spektroskopie kann dann eine Alternative darstellen, wenn Moleküle bzw. ihre Schwingungen im IR-Spektrum schlecht nachweisbar sind, wobei die Raman-Spektroskopie ein dichtes Medium (Flüssigkeit, Feststoff) voraussetzt. Gut nachweisen lassen sich symmetrische Moleküle und Ionen. Ein Vorteil liegt auch darin, dass Wasser die Messung nicht stört, was es für den Einsatz in der Emulsionspolymerisation interessant macht. Die Messung erfolgt durch ein Fenster in der Außenwand und nicht im Medium selbst. Die Signalübertragung kann mittels Lichtwellenleiter stattfinden, wobei Störungen durch Fluoreszenz möglich sind.
- Terahertzspektroskopie: PE, PP, Teflon, aber auch Karton und div. Textilien sind im Gegensatz zu Metallen für Terahertzstrahlung vollständig transparent und weisen eine hohe Eindringtiefe und gute räumliche Auflösung auf. Dies macht die Technik interessant für nichtinvasive Inline-Messverfahren sowie dreidimensionale Tomographie. Ihre Verwendung ist außerdem unabhängig vom Aggregatzustand des Mediums. THz-Strahlung regt vor allem schwache Bindungstypen (Wasserstoffbrücken, VdW-Bindungen) an und eignet sich für große und komplexe Moleküle, wie z. B. biologische Makromoleküle. Da Wasser die Strahlung absorbiert, ist auch eine Bestimmung der Restfeuchte möglich.
- Transmissions-Spektroskopie (UV/Vis-Bereich): Die UV/Vis-Spektroskopie eignet sich sowohl in Flüssigkeiten als auch in Gasen zur Konzentrationsbestimmung (z. B. Aromaten, Nitroverbindungen, Chlor, Ozon, Nitrit etc.), zur Farbzahlbestimmung und zur Trübungsmessung. Es werden entweder Lichtwellenleiter verwendet oder Quarz-, Borosilikat- oder Saphirfenster direkt in die Rohrleitung eingesetzt. Unter 250 nm können Lichtwellenleiter auf Grund des Solarisationseffekts nur eingeschränkt verwendet werden. Aus Gründen der Robustheit und der Messgeschwindigkeit kommen hauptsächlich Diodenarray-Spektrometer zum Einsatz. Für Trübungsmessungen werden Photometer mit zwei Detektoren in unterschiedlichen Winkeln verwendet.
- Ultraschall-Messtechnik: Gemessen wird die Ausbreitungsgeschwindigkeit des Schalls im Medium. Diese ist abhängig von diversen Stoffparametern – Druck, Temperatur, Viskosität, Dichte, Zusammensetzung, Kompressibilität, Strömungsgeschwindigkeit – und kann somit für die Bestimmung eben dieser eingesetzt werden. Für Konzentrationsmessungen ist der Einsatz jedoch auf binäre bzw. quasibinäre Systeme beschränkt. Es gibt Messköpfe für invasive, wie nichtinvasive Messungen in flüssigen Medien. Für eine korrekte Auswertung ist ein Kennlinienfeld zu vermessen und mit den Messwerten zu verrechnen. Insbesondere der Temperatureinfluss muss hier korrigiert werden.
|
ATR-Spektroskopie |
Gase, |
invasiv |
Konzentration |
mehrere Messstellen |
|
IR-Spektroskopie |
Flüssigkeiten |
invasiv |
Konzentration: |
Stoffidentifikation, |
|
Laser-Spektroskopie |
Gase |
nicht-invasiv |
Konzentration: |
Hochtemperaturbereich |
|
Raman-Spektroskopie |
Feststoffe, |
nicht-invasiv |
Konzentration: |
Messung in Emulsionen |
|
Therahertz-Spektroskopie |
Feststoffe, |
nicht-invasiv |
Konzentration: |
2-D-Imaging, |
|
Transmissions- |
Flüssigkeiten, |
invasiv/ |
Konzentration: |
Trübungsmessungen |
|
Ultraschall |
Flüssigkeiten |
invasiv/ |
Konzentration: |
Stoffidentifikation |
Quelle(n):
- Kasten, W. (2008): Neue Entwicklungen auf dem Gebiet der Inline-Prozessanalysetechnik. atp edition, Heft 9 S. 58 ff.
Modell- und Algorithmen-basierte Prozessdatenauswertung
Auch die kombinierte Auswertung der Sensordaten mithilfe mathematischer Modelle und Algorithmen ermöglicht neue Erkenntnisse. So können kritische Kenntnislücken geschlossen und durch modellbasierte Vorhersagen Prozesse auf Parameter hin optimiert werden, die nicht direkt für Messungen zugänglich sind [DECHEMA (2020)].
Quelle(n):
- DECHEMA (2020): Prozessanalytik – Rasante Entwicklung eines Wegbereiters [online]. DECHEMA – Gesellschaft für chemische Technik und Biotechnologie e.V., 06.02.2020 [abgerufen am: 11.02.2020], verfügbar unter: Link
Online-Sensorsysteme
Online-Sensorsysteme stellen für biotechnologische Produktionsprozesse ein zentrales Element der Bioprozesskontrolle dar. Sie tragen entscheidend dazu bei, dass ein Bioprozess ressourceneffizient und mit minimaler Fehlchargen-Anzahl das Produktionsziel erreicht. Für eine optimale Bioprozesskontrolle sind biochemische Leitgrößen notwendig, die allerdings für eine direkte Messung nicht zugänglich sind. Alternativ werden durch indirekte Messmethoden Datenmengen anderer Prozessgrößen ermittelt, aus denen sich anhand intelligenter Auswertungsalgorithmen relevante Informationen über den Prozesszustand gewinnen lassen [Wiechert, W. et al. (2018), S. 8].
Neben der Bestimmung der klassischen Prozessparameter wie Temperatur, Druck und pH-Wert kommen für die Detektion von Stoffeigenschaften in erster Linie spektroskopische Methoden wie UV/VIS, IR oder NMR in der Prozessanalytik in biotechnologischen Verfahren zum Einsatz.
Tendenzen hin zu immer kompakteren Messsystemen (Miniaturisierung) sowie der große Fortschritt in der Lasertechnologie und im Detektordesign haben den Einsatzbereich dieser Analysemethoden stark erweitert. Die oftmals komplizierte Integration der Sensorik wird durch die Kombination mit „intelligenter“ Software (intelligenten Sensoren) möglich. Sie stellt die automatische Nachkalibrierung und damit deutlich längere Laufzeiten bereit [DECHEMA (2020)]. Darüber hinaus sind intelligente Sensorsysteme in der Lage, eine Selbstüberwachung und -diagnose, eine integrierte Datenauswertung mit Logik- und Regelungsfunktionalität oder eine interaktive Vernetzung mit anderen Komponenten im Prozessumfeld durchzuführen [Wiechert, W. et al. (2018), S. 8].
Quelle(n):
- Wiechert, W.; Scheper, T. und Weuster-Botz, D. (2018): Neue Schubkraft für die Biotechnologie – Miniaturisierung, Automatisierung und Digitalisierung revolutionieren die Entwicklung biotechnologischer Prozesse und Produkte. DECHEMA Gesellschaft für Chemische Technik und Biotechnologie e.V., Frankfurt am Main [abgerufen am: 12.12.2019], verfügbar unter: Link
- DECHEMA (2020): Prozessanalytik – Rasante Entwicklung eines Wegbereiters [online]. DECHEMA – Gesellschaft für chemische Technik und Biotechnologie e.V., 06.02.2020 [abgerufen am: 11.02.2020], verfügbar unter: Link
Optimierte Basisregelung
Die effiziente Nutzung der verwendeten Ressourcen (Stoffströme und Energie) in einem Prozess wird unter anderem durch die eingesetzte Basisregelung bestimmt. Eine bestehende Basisregelung sollte regelmäßig vom Anlagenbediener hinsichtlich der Erfüllung der Regelaufgabe (z. B. „geringes Schwingen" der Regelgröße, keine Störung der Folgeprozessschritte) bewertet werden. Insbesondere sollte geprüft werden, ob die gewählten Regel- und Stellgrößen sowie der Sollwert dazu geeignet sind, die Zielstellung der Regelaufgabe zu erfüllen. Eine Nichterfüllung der Regelaufgabe kann durch folgende Maßnahmen korrigiert werden:
- Änderung der gewählten Regel-, Stellgrößen und/oder Sollwerte
- Änderung der eingesetzten Regelstruktur hin zu einer komplexeren Struktur (z. B. Kaskadenregelung)
Voraussetzung für das Erkennen einer ungünstigen Regelstruktur während des Anlagenbetriebs durch ein fachgerechtes Reglermonitoring ist eine gewisse Beurteilungskompetenz der Anlagenfahrer. Diese kann durch regelmäßige Schulungen gefördert und auf den aktuellsten Stand gebracht werden. Um schon zu Beginn der Betriebsphase ungünstige Regelstrukturen zu verhindern, sollten bereits während der Anlagenplanungsphase Prozessführungsingenieure oder Ingenieure mit Prozessführungserfahrung beteiligt werden.
Praxisbeispiel(e) finden Sie unter www.namur.net/uploads/tx_press/atp_02_2008_Prozessfuehrung.pdf (S. 70 f.).
Quelle(n):
- Hagenmeyer, V. und Piechottka, U. (2009): Innovative Prozessführung – Erfahrung und Perspektiven. atp edition, Heft 1-2 S. 52
Partikel-/Tropfengröße
Die Kenntnis über die Partikel- oder Tropfengrößenverteilung und die damit einhergehende Größe der Phasengrenzfläche ist entscheidend bei der Steuerung und Regelung disperser Reaktions- oder Prozesssysteme. Eine schnelle Analyse der dispersen Phase ermöglicht die Minimierung von Materialeinsatz, Energieeintrag und/oder Abfallprodukten. Folgende Technologien werden zur Bestimmung von Partikel- oder Tropfengröße und -konzentration eingesetzt:
- Photo-optische Inline-Messtechnik (inklusive innovativer Bildbearbeitungssoftware)
- Diverse Lasermesstechniken wie z. B. Laserbeugung, Photonendichtewellen-Spektroskopie
- Photo-Sonden wie z. B. Endoskope, Mikroskope
Quelle(n):
- Kraume, M. und Maaß, S. (2012): Prozesse auf Basis der Partikelgröße steuern. CITplus, 15. Jahrgang, 05. Jun. 2012, Ausgabe 6 S. 31-33
- Reich, O.; Bressel, L.; Hass, R. und Münzberg, M. (2012): Prozessanalyse stark lichtstreuender Dispersionen mit Photonendichtewellen-Spektroskopie. Chemie Ingenieur Technik, 84, Nr. 8
pH-Wert
Bei vielen chemischen Reaktionen beeinflusst der pH-Wert den Reaktionsverlauf (z. B. Reaktionsgeschwindigkeit, Gleichgewicht). Ein Monitoring des pH-Werts unterstützt daher eine optimierte Reaktionsführung, was i. d. R. zu einem effizienten Stoffeinsatz führt. Für den Einsatz im technischen Prozess werden Einstab-Elektroden, bestehend aus Bezugs- und Messelektrode, eingesetzt. Mit ihnen sind kontinuierliche Messungen möglich. Sie sind fest in einer Rohrleitung oder einem Apparat (z. B. Reaktor) installiert.
Quelle(n):
- Ignatowitz, E. (2013): Chemietechnik. 11. Auflage, Verlag Europa-Lehrmittel, Haan-Gruiten. S. 283 f.
Prozessanalytik
Die Prozessanalytik (PAT) bildet den Kern vieler innovativer Technologien (z. B. Predictive Control). Die PAT ist dabei ein multidisziplinäres Thema: angefangen bei der analytischen Methodik über die Entwicklung neuer Sensoren bis hin zur Integration von Daten aus verschiedenen Quellen und Rückkopplungsschleifen. Dies erfordert die Zusammenarbeit von Ingenieuren, Chemikern und Datenwissenschaftlern [DECHEMA (2020)].
Der Einsatz von Prozessanalytik und -steuerung in Bioprozessen ist mit besonderen messtechnischen Herausforderungen konfrontiert: der komplexen Zusammensetzung des Produktgemisches bestehend aus nicht umgesetzten Reaktanten, Produkten und Nebenprodukten sowie insgesamt geringen Konzentrationen der zu detektierenden Substanzen. Des Weiteren sind die zu detektierenden Substanzen im Reaktor nicht gleichverteilt (Inhomogenitäten). Hinzu kommt eine gewisse Varianz in der Zusammensetzung und Qualität der Rohstoffe (Reaktanten).
Für die Implementierung von Bioprozessen in der chemischen Industrie sind Entwicklungen von fortschrittlichen Analyse- und Steuerungstechnologien entscheidend. Hierzu ist der Übergang von Batch- zu kontinuierlichen Analyse- und Steuerungsprozessen notwendig. Voraussetzung ist ein sehr gutes Prozessverständnis bezogen auf den gesamten Prozesszeitraum. Der Vorteil besteht in einer Kontrolle der Qualität in Echtzeit und einer zeitnahen Anpassung der Prozessparameter [DECHEMA (2020)].
Quelle(n):
- DECHEMA (2020): Prozessanalytik – Rasante Entwicklung eines Wegbereiters [online]. DECHEMA – Gesellschaft für chemische Technik und Biotechnologie e.V., 06.02.2020 [abgerufen am: 11.02.2020], verfügbar unter: Link
Prozessdiagnose
Bei einer Prozessdiagnose erfolgt das Erkennen kritischer Zustände und Störungen durch die Erfassung, Überwachung und Bewertung relevanter Prozessgrößen. Dazu werden Soll- und Ist-Zustände online und in Echtzeit miteinander verglichen, um gegebenenfalls mit Mitteln der Prozessführung auf identifizierte Störungen zu reagieren. Neben der Diagnose des Prozesszustandes werden in der Regel Informationen zum Zustand und Verhalten der eingesetzten Anlagenkomponenten gewonnen. Die für die Prozessführung und Regelung eingesetzten Feldgeräte (Sensoren, Regler etc.) und deren Messdaten können für die Prozessdiagnose genutzt werden.
Praxisbeispiele:
- Regelgüteauswertung: Die Aufzeichnung und Auswertung relevanter Reglerdaten wie Soll- und Istwerte, Stellgrößen erlauben z. B. mit Hilfe grafischer Darstellungsmethoden die Beurteilung der eingesetzten Regelkreise. Dadurch können nicht optimal eingestellte Regler oder fehlerhafte Stellglieder (z. B. Ventile) leicht identifiziert und Lösungsvorschläge erarbeitet werden. Die Datenerfassung erfolgt in der Regel mit Hilfe des Prozessleit- (PLS) und Prozessinformationsmanagementsystems (PIMS).
- Fingerabdruck-Methode für Batchreaktoren: Um den Reaktionsverlauf eines Batches ad hoc beurteilen zu können, werden im Rahmen dieser Methode eine große Anzahl bereits absolvierter Batchversuche ausgewertet. Alle hinsichtlich Zeit- und Umsatzentwicklung gut verlaufenden Batches werden zusammen in einem typischen Diagrammtyp (z. B. Zeit, Umsatz) dargestellt. Dabei wird ein Reaktionsverlaufsbereich, welcher durch eine obere und untere Verlaufsgrenze markiert ist, ermittelt. Alle Reaktionsverläufe, die innerhalb dieses Bereichs liegen, werden für gut befunden. Alle außerhalb der Bereichsgrenze liegenden Verläufe entsprechen nicht den Vorgaben und sollten aus ökonomischen und ökologischen Gründen abgebrochen werden. Mit dieser Methode werden dem Anlagenfahrer eine sofortige Beurteilung der Verlaufsgüte eines Batches sowie schnelles Handeln ermöglicht.
- Ein weiteres Praxisbeispiel finden Sie unter www.namur.net/uploads/tx_press/atp_02_2008_Prozessfuehrung.pdf (S. 76).
Im Bereich Prozessdiagnose besteht ein großes Potenzial zur Steigerung der Energieeffizienz. Die zurzeit angewendeten Methoden und Tools sollten anwendungsorientierter und funktionaler werden. Zudem sollten sie leichter in die vorhandenen Automatisierungssysteme integrierbar sein.
Quelle(n):
- Hagenmeyer, V. und Piechottka, U. (2009): Innovative Prozessführung – Erfahrung und Perspektiven. atp edition, Heft 1-2 S. 59 ff.
- Krämer, S.; Bamberg, A.; Dünnebier, G.; Hagenmeyer, V.; Piechottka, U. und Schmitz, S. (2008): Prozessführung: Beispiele, Erfahrung und Entwicklung. atp edition, Heft 2 S. 76 ff.
Sensorkalibrierung
Durch Sensoren generierte Messwerte bilden häufig entscheidende Inputgrößen für Prozessführungsstrategien. Um Fehlentscheidungen vorzubeugen, die zu ungünstigen Betriebspunkten und damit zu erhöhtem Energie- oder Stoffverbrauch führen könnten, ist das Auftreten von Messfehlern zu verhindern. Durch regelmäßiges Kalibrieren der Sensoren wird eine Messung außerhalb der vorgegebenen Toleranzbereiche und somit das Auftreten von Messfehlern verhindert. Sinnvolle Kalibrierabstände werden in der Regel vom Sensorhersteller festgelegt und in der Betriebsanweisung kommuniziert. Eine Dokumentation der Kalibrierdaten (z. B. Kalibrierfunktion) ist sinnvoll, da aus der Kalibrierhistorie diverse Überprüfungen und damit verbundene Rückschlüsse möglich sind:
- Alterung des Sensors (Sensoraustausch)
- Überprüfung der Kalibrierabstände (Verlängerung oder Verkürzung)
Viskosität
Anhand der Messgröße Viskosität kann die Fließfähigkeit einer Flüssigkeit beschrieben und beurteilt werden. Die Viskosität stellt für die Qualitätssicherung und Prozessführung eine wichtige Größe dar. Folgende Messgeräte stehen zur Verfügung:
Höppler-Kugelfall-Viskosimeter
- Nur für diskontinuierliche Messung geeignet; Probenahme notwendig
- Nur für transparente Flüssigkeiten einsetzbar
- Messvorgang dauert einige Minuten
- Messwertnahme und Viskositätsberechnung erfolgen manuell
- Ohne Hilfsenergie
- Einsatz im Labor und im Betrieb
Rotationsviskosimeter
- Zwei Geräteausführungen möglich:
- Diskontinuierliche Rotationsviskosimeter mit Probenahme für Laboreinsatz
- Kontinuierliche Rotationsviskosimeter für Inline-Messung direkt in Rohrleitung einer Anlage - (Elektrische) Hilfsenergie notwendig
- Viskosität wird geräteintern berechnet und im Display angezeigt
- Einsatz in Prozesssteuerung und Qualitätssicherung
Kapillar-Viskosimeter
- Zwei Geräteausführungen möglich:
- Diskontinuierliche Kapillar-Viskosimeter mit Probenahme für Laboreinsatz
- Bei einem kontinuierlichen Kapillar-Viskosimeter wird in regelmäßigen Intervallen eine Probe des Messmediums (z. B. aus Rohrleitung) in das Viskosimeter geleitet - (Elektrische) Hilfsenergie notwendig
- Viskosität wird geräteintern berechnet und im Display angezeigt
- Einsatz in Prozesssteuerung und Qualitätssicherung
Quelle(n):
- Ignatowitz, E. (2013): Chemietechnik. 11. Auflage, Verlag Europa-Lehrmittel, Haan-Gruiten. S. 282 f.
Projekte
WiPro – Wissensbasierte Prozessintelligenz Teilprojekt K: Populationsdynamiken als Biosensoren für biotechnische Prozesszustände
- Neue Wege zu stabilen Bioprozessen: Realisierung und Bereitstellung einer Plattform (multimodalen Sensor- und Software-Plattform) zur Kontrolle und Steuerung von biotechnologischen Prozessen
- Verwenden optischer Informationen von mikrobiellen Organismen zur nachhaltigen Steuerung und Optimierung biotechnischer Prozesse
- Hardware-Anpassung des vorhandenen Benchtop Flow Zytometers
- Weiterentwicklung bioinformatischer Tools zur Auswertung und Interpolation großer zytometrischer Datensätze
- Erstellen eines Interfaces zwischen Zytometer und bioinformatischen Tools
- Untersuchen der Einflussfaktoren auf die Leistungsfähigkeit mikrobieller Systeme
Robustes Automatisierungskonzept für die Produktion von Algenbiomasse im Freiland
- Hohes Potenzial der Nutzung von Öl aus Mikroalgen als Biokraftstoff durch den großen Ertrag pro Fläche und den verminderten Wasserverbrauch bei der Kultivierung
- Entwicklung einer standardisierten Prozessautomatisierung für die Kultivierung von Mikroalgen zur Anwendung im technischen Maßstab
- Prozessteuerung ausschließlich basierend auf pH-Wert- und Reaktortemperatur-Messung: Regelung des pH-Werts über den CO2-Anteil in der Zuluft und Rückschließen auf Ammoniumkonzentration
- Etablierung eines stabilen Wachstumsprozesses im Freiland mit einer durchschnittlichen Biomassekonzentration von 8,5 g/L
SensoSpheres – Ortsungebundene Aufnahme von Prozessmesssignalen in neuartigen Bioreaktorsystemen
- Entwicklung eines ortsunabhängigen Miniatur-Messsystems für Bioreaktoren: mobiler Sensor in Gestalt einer kleinen Kugel
- Selbstständige Erfassung von Prozessparametern (z. B. Temperatur der Bioreaktorflüssigkeit) sowie Übertragung und Auswertung der Messdaten an eine Basisstation
- Miniatur-Messsystem entspricht einer Sensorkugel mit 7,8 mm im Durchmesser
- Durch das nichtstarre Messsystem ist eine präzisere Erfassung der tatsächlichen Prozessbedingungen möglich und somit ist der Prozess effizienter steuerbar
WiPro – Wissensbasierte Prozessintelligenz Teilprojekt A: Software-Plattform für Multi-/Single-Use-Bioreaktoren
- Entwicklung und Umsetzung einer multimodalen Sensor- und Software-Plattform zur Überwachung und Steuerung von biotechnologischen Prozessen
- Kombination von Software und Sensortechnik in einer digitalen Plattform zur gesamtheitlichen qualitativen Prozessbeurteilung
- Entwicklung eines Automatisierungskonzepts für die Software-Plattform nach Bewertung der vorhandenen Marktsituation
- Implementierung etablierter Schnittstellen zum Anschließen der Sensoren an die Software-Plattform
- Zusammenstellen von Informationen zu ökonomischen und ökologischen Prozess- und Produktionskenngrößen
- Ziel der Reproduzierbarkeit von Bioprozessen durch Prozessautomatisierung
WiPro – Wissensbasierte Prozessintelligenz Teilprojekt B
- Entwicklung eines ultraschallbasierten Sensorkonzepts zur Bestimmung der Biomassekonzentration
- Untersuchen der Einsatzmöglichkeit zur Abschätzung von Partikelgrößen in Suspensionen
- Fokussierung auf Hygienic Design, Online-Fähigkeit und Übertragbarkeit des Systems auf weitere biotechnologische Prozesse
- Messen von Schallgeschwindigkeit und Dämpfung sowie anschließende Verknüpfung mit akustischer Theorie
- Optimierung der Auswertealgorithmen durch Vergleich mit Referenzmessungen
- Ermöglichung einer In-situ-Messung mit Sensorkonzept aus Messzelle, Transducern und entsprechender Signalanregung/-aufzeichnung
WiPro – Wissensbasierte Prozessintelligenz Teilprojekt C: Entwicklung und Charakterisierung einer miniaturisierten Probenahmesonde für die Single-Use-Bioprozesstechnik
- Entwicklung und Charakterisierung einer miniaturisierten Probenahmesonde für die Single-Use-Bioprozesstechnik
- Auswahl und Charakterisierung von neuen Membranteilen für den Einsatz als Trennmaterial in Filtrationssonden
- Entwicklung und Konstruktion neuer Sondentypen für den Einsatz in der Einweg-Bioprozesstechnik
- Einsatz der Sondenprototypen in realen Fermentationen und Zellkultvierung im Anschluss an Labortests
WiPro – Wissensbasierte Prozessintelligenz Teilprojekt F: "BlueCart" (Austauschbare Sensorkartuschen für Gassensoren)
- Neue Wege zu stabilen Bioprozessen: Realisierung und Bereitstellung einer Plattform (multimodalen Sensor- und Software-Plattform) zur Kontrolle und Steuerung von biotechnologischen Prozessen
- Entwicklung austauschbarer Sensorkartuschen für Gase
- Sensoren basieren auf Infrarotmesstechnik
- Justierbarkeit der Sensoren für jede Gaskonzentration soll ohne zusätzliche Hilfsmittel möglich sein
- Ermöglichen des Wechselns der Kartusche ohne Sensoraustausch
- Entwicklung einer stabilen, resistenten Membran mit guten Diffusionseigenschaften für Gase zum Einsatz in IR-Ethanol-/Methanolsensoren mit geringer Baugröße
WiPro – Wissensbasierte Prozessintelligenz Teilprojekt H: Entwicklung von optischen Glucosesensoren für die Biotechnologie
- Neue Wege zu stabilen Bioprozessen: Realisierung und Bereitstellung einer Plattform (multimodalen Sensor- und Software-Plattform) zur Kontrolle und Steuerung von biotechnologischen Prozessen
- Entwicklung eines optischen, enzymatischen Glucosesensors für die Online-Erfassung der Glucosekonzentration
- Universell einsatzbares Sensorsystem inkl. Messverstärker zur Detektion und Quantifizierung von Glucose
- Messung unter unterschiedlichen Bedingungen möglich (Temperatur, Sauerstoffkonzentration)
- Keine negative Beeinflussung des biologischen Prozesses, da nicht cytotoxisch
- Implementierbar in übergeordnete Prozessleitstrukturen
WiPro – Wissensbasierte Prozessintelligenz Teilprojekt J: Entwicklung und Realisierung eines multimodalen Messsystems
- Evaluierung neuer Konzepte zur Bioprozesskontrolle und Bioprozesssteuerung
- Evaluierung, Implementierung und Qualifizierung neuartiger Sensoren
- Evaluierung mathematisch-statistischer Auswertemethoden
- Feldtests der Implementierungen an tierischen Zellstrukturen und mikrobiellen Fermentationen
- Plausibilitätsprüfung der einzelnen Sensordaten durch Verknüpfung der Sensorergebnisse mit den entsprechenden Reaktorparametern
- Entwerfen neuartiger Integrationsmöglichkeiten zum Einsatz von Sensoren in Einweg-Biokatalysatoren bei der Herstellung von Biopharmazeutika
- Konzeption von Single-Use-Biokatalysatoren zum Einsatz in der mikrobiellen Fermentation
- Aufbau eines Netzwerks aus etablierter und neuer Sensorik
WiPro – Wissensbasierte Prozessintelligenz Teilprojekt L: Datensammlung und Auswertung mit SIPAT
- Neue Wege zu stabilen Bioprozessen: Realisierung und Bereitstellung einer Plattform (multimodalen Sensor- und Software-Plattform) zur Kontrolle und Steuerung von biotechnologischen Prozessen
- Optimierte Auswertung von Prozessdaten durch eine konsistente Erfassung aller Daten in SIPAT
- Bewertung neuartiger Sensortechnologien hinsichtlich der Integrierbarkeit in eine Automatisierungsplattform für Bioprozesse
- Verbesserung des Prozessverständnisses und der Produktqualität durch Anwendung von Advanced-Process-Control-Strategien
- Sicherstellen der Übertragbarkeit des Gesamtkonzepts in das industrielle Umfeld
Wissensbasierte Prozessintelligenz
- 20 Partner haben sich zu Bündnis "Wissensbasierte Prozessintelligenz" formiert
- Ziel: besseres Monitoring von Prozessen der Bioproduktion zum Erlangen eines besseren Prozessverständnisses
- Durch höhere Prozesssicherheit sollen eingesetzte Ressourcen effizienter genutzt werden
Rohstoffaufbereitung
Gute Praxis
Lignocellulosehaltige Biomasse – Herausforderungen
Lignocellulosehaltige Biomasse zeichnet sich durch eine sehr gute Verfügbarkeit, vergleichsweise geringe Herstellungskosten und fehlende Konkurrenz zu Lebens- und Futtermitteln aus. Allerdings müssen bei der Nutzung lignocellulosehaltiger Biomasse in Bioprozessen einige Herausforderungen bewältigt werden wie beispielsweise [Nusser, M. et al. (2007), S. 43]
- die Entwicklung von kosteneffizienten Verfahren, die einen material- und energieeffizienten Aufschluss der Lignocellulose ohne Freisetzung und Bildung von Hemmstoffen ermöglichen,
- die vollständige Umsetzung der aus den Aufschlussverfahren enthaltenen Zucker (z. B. Hexosen, Pentosen) zu den gewünschten Produkten in ressourceneffizienten Verfahren,
- die Produktabtrennung in einem ressourcen- und kosteneffizienten Verfahren,
- die Integration von Aufschluss-, Umsetzungs- und Produkttrennungsverfahren in einem Gesamtverfahren sowie der Nutzung bzw. Kreislaufführung aller anfallenden Reststoffe.
Quelle(n):
- Nusser, M.; Hüsing, B. und Wydra, S. (2007): Potenzialanalyse der industriellen, weißen Biotechnologie. Fraunhofer-Institut für System- und Innovationsforschung (Fraunhofer ISI), Karlsruhe.
Lignocellulosehaltige Biomasse – Vorteile
Lignocellulosehaltige Biomasse als Substrat für Bioprozesse hat gegenüber stärke- und zuckerhaltigen Substraten diverse Vorteile. Ein Hauptvorteil liegt darin, dass sie aufgrund der Unverdaulichkeit für den tierischen Organismus nicht mit Lebens- und Futtermitteln konkurriert. Darüber hinaus ist Lignocellulose in großen Mengen und vielfältiger Form verfügbar, beispielsweise in Form von landwirtschaftlichen Reststoffen (z. B. Stroh, Maispflanzen), festen Siedlungsabfällen, industriellen Produktionsrückständen oder Industriepflanzen (z. B. Einjahrespflanzen). Dies resultiert in niedrigen Biomasse-Herstellungskosten (Substratkosten). Des Weiteren ist der für Bioprozesse nutzbare Wertstoffanteil in lignocellulosehaltiger Biomasse größer verglichen mit stärke- und zuckerhaltiger Biomasse [Nusser, M. et al. (2007), S. 43].
Quelle(n):
- Nusser, M.; Hüsing, B. und Wydra, S. (2007): Potenzialanalyse der industriellen, weißen Biotechnologie. Fraunhofer-Institut für System- und Innovationsforschung (Fraunhofer ISI), Karlsruhe.
Nutzungswege von Biomasse als Rohstoff
Der Rohstoff Biomasse wird aus einem komplexen Stoffgemisch gebildet. Um die hierin enthaltenen Stoffe zu nutzen, bedarf es einer Aufarbeitung zur Gewinnung der Wertstoffe mit einer anschließenden Umsetzung zu Produkten. Dies kann auf unterschiedlichen Wegen erfolgen [Nusser, M. et al. (2007), S. 42]:
- Es gibt bereits in der Biomasse vorliegende Wertstofffraktionen (z. B. sekundäre Pflanzenstoffe), die mittels effizienter Extraktionsverfahren herauslösbar sind. Die somit gewonnenen natürlichen chemischen Strukturen können entweder direkt oder mit leichten chemischen Modifikationen in anderen Produkten wie beispielsweise aus der Lebensmittelindustrie eingesetzt werden.
- Die Biomasse kann einerseits direkt mittels geeigneter Aufbereitungs- und Biokonversionsverfahren zu Plattformchemikalien umgesetzt werden, aus welchen dann weitverzweigte Produktbäume erschließbar sind. Anderseits kann die Biomasse in ihre (einheitlichen) Bausteine zerlegt werden. Aus den erhaltenen Bausteinen (z. B. Methan) werden dann die gewünschten Produktmoleküle synthetisiert.
Quelle(n):
- Nusser, M.; Hüsing, B. und Wydra, S. (2007): Potenzialanalyse der industriellen, weißen Biotechnologie. Fraunhofer-Institut für System- und Innovationsforschung (Fraunhofer ISI), Karlsruhe.
Verfahren
Um die Biomasse in fermentierbare bzw. biokatalytisch zugängliche Substrate zu überführen, muss ein Aufschlussverfahren durchgeführt werden. Abhängig von der Komplexität des biobasierten Ausgangsstoffes ist dieses Aufschlussverfahren ein- oder mehrstufig gestaltet. Bei den zur Auswahl stehenden Ausschlussverfahren handelt es sich um chemische, thermische und mechanische Verfahren. Während des Rohstoffaufbereitungsprozesses können mehrere Stoffströme entstehen, die für verschiedene Verwertungsstrategien geeignet sein können [Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB (kein Datum), S. 5].
Nach Ermittlung der genauen stofflichen Zusammensetzung der Biomasse wird die Entwicklung des Aufschlussverfahrens mit dem Ziel durchgeführt, die Biomassebestandteile in „optimaler“ Substratform den Mikroorganismen (Fermentation) bzw. Enzymen (Biokatalyse) zur Verfügung zu stellen. Bei etwas komplexeren Aufschlussvorhaben kann auch auf eine Kombination von Verfahren zurückgegriffen werden. Ein im Vorfeld der Aufschlussverfahrensentwicklung durchgeführtes Substratengineering hilft dabei zu ermitteln, was der Aufschlussprozess leisten muss. Dabei wird beispielsweise die optimale Zusammensetzung der Stoffströme für nachfolgende Prozessschritte ermittelt und festgelegt oder mögliche Hemmstoffe werden identifiziert und das Verfahren für eine Entfernung bestimmt [Nusser, M. et al. (2007), S. 44 f.].
Quelle(n):
- Nusser, M.; Hüsing, B. und Wydra, S. (2007): Potenzialanalyse der industriellen, weißen Biotechnologie. Fraunhofer-Institut für System- und Innovationsforschung (Fraunhofer ISI), Karlsruhe.
- Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB (kein Datum): Industrielle Biotechnologie – Die Natur als chemische Fabrik. Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB, Stuttgart [abgerufen am: 07.01.2020], verfügbar unter: Link
Projekte
Mikrobielle Laugung als Recycling-Verfahren für Seltene Erden
- Erweiterung der Ausnutzung mikrobiologischer Stoffwechselprozesse auf die Rückgewinnung von seltenen Erden aus elektronischen Abfallprodukten
- Erprobung der Solubilisierung von seltenen Erden in Oxidform und Phosphaten mithilfe von Mikroorganismen anhand von Modellverbindungen
- Analyse von 18 verschiedenen mikrobiellen Stämmen (Bakterien und Hefen) für die organische Säureproduktion
- Lösen von mehr als 12 % der seltenen Erden mithilfe von Mischkulturen
Videos
Ein Netz aus Wärme
Mit dem Aufruf des Videos erklären Sie sich einverstanden, dass Ihre Daten an YouTube übermittelt werden und dass Sie die Datenschutzerklärung gelesen haben.
Biokonversion
Gute Praxis
Mikrobielle Elektrosynthese
Um unabhängiger von der klimaschädlichen Erdölförderung zu werden, versucht das Dechema-Forschungsinstitut (DFI) das Synthetisieren von kurzkettigen Kohlenstoffverbindungen aus Kohlendioxid mithilfe der „Biologisierung der Chemie“ effizienter zu machen. Bislang scheiterte die industrielle Umsetzung der elektrochemischen Synthetisierung von Kohlenstoffverbindungen vor allem an zu geringen Wirkungsgraden der Reaktionen. Ein neu entwickelter Prozess, die sogenannte „mikrobielle Elektrosynthese“, verspricht jetzt eine ressourcenschonende und ökologisch kompatible alternative Lösung. Statt allein auf elektrochemische Prozesse, setzt die mikrobielle Elektrosynthese auf einen kombinierten Ansatz, bei dem ein Film von Bakterien auf die Elektroden aufgebracht wird. Diese Bakterien nehmen dann die Elektronen auf und setzen dabei Kohlendioxid zu Methan um. Der Vorteil liegt in der hohen Prozesseffizienz, mit der die Bakterien diese Synthetisierung ausführen [Schrader, J. (2017)].
Quelle(n):
- Schrader, J. (2017): An den Grenzen der Fachgebiete – Das Dechema-Forschungsinstitut entwickelt übergreifende Lösungskonzepte aus den Themengebieten Chemische Technik, Werkstoffe und Biotechnologie. In: CITplus, (7-8), 52 – 53.
Projekte
Bakterien recyceln Platingruppenmetalle und produzieren Umweltkatalysatoren zur Entfernung von langlebigen organischen Schadstoffen
- Entwicklung von (bio-)metallurgischen Methoden für die nachhaltige Rückgewinnung von Edelmetallen
- Verwendung von Schwermetall-toleranten Bakterien als Produzenten von hochaktiven Nanokatalysatoren in Form von Edelmetall-Nanopartikeln
- Simultaner Ablauf des mikrobiellen Wachstums, der Metallreduktion und der Nanopartikel-Bildung durch biotechnologischen Prozess
Biokatalysatoren in Bioreaktoren: Monitoring, Regelung und multikriterielle Optimierung von Biogasprozessen; Teilvorhaben 1: Einsatz und Wirkung der Biokatalysatoren
- Entwicklung von Strategien zur Unterstützung der Hydrolyse von nachwachsenden Rohstoffen mittels der gezielten Zugabe von ergänzenden Enzymen pilzlichen Ursprungs
- Charakterisierung mikrobieller Stoffwechselaktivitäten in semi-kontinuierlich betriebenen Biogasreaktoren
- Untersuchung stofflicher Vorgänge beim Lignocelluloseabbau
- Untersuchung der Wirkung von Biokatalysatoren auf die Stoffwechsel- und Abbauvorgänge durch die Erfassung chemischer, biochemischer, rheologischer und technischer Parameter
ECOX – Enzymatisch-chemokatalytische Oxidationskaskaden in der Gasphase
- Etablierung eines enzymatisch-chemokatalytischen Prozesses zur stofflichen Nutzung von Methan aus Biogas
- Kombination chemischer und enzymatischer Prozessschritte zur effizienten Umsetzung von Methan zu Methanol und Ameisensäure
- Entwicklung des Prozesses als Grundlage für die Nutzung von Biogas als Kohlenstoffquelle anstelle der Verbrennung zur Energiegewinnung
- Charakterisierung und Optimierung der Enzyme durch katalytische Parameter (pH- und Temperatur-Optimum)
- Gezieltes Verändern der Enzyme zum Ermöglichen der Aufbringung auf verschiedene Trägermaterialien
- Entwicklung stabiler, mehrfach verwendbarer Katalysatoren für einen effizienten Prozess
ECOX2 – Enzymatische und chemokatalytische Oxidationskaskade in der Gasphase (2) – Phenol aus Biogas
- Entwicklung eines chemokatalytisch-biotechnologischen Verfahrens zur Herstellung von Phenol aus Methan (Biogas)
- Erster Schritt: chemokatalytische Herstellung von Benzol und den Nebenprodukten Ethen und Naphthalin aus Biogas
- Zweiter Schritt: Entwicklung einer Fermentationstechnik zur biotechnologischen Umsetzung von Benzol in Phenol mithilfe von methanoxidierenden Bakterien sowie Umsetzung der Nebenprodukte in Ethylenoxid und Naphthol mittels einer Bioreaktorkaskade
Herstellung von Fumarsäure zur Polymeranwendung
- Entwicklung eines effizienten und wirtschaftlichen Biokonversionsprozesses für Fumarsäure
- Etablierung eines biokatalytischen Weges zur Herstellung von Fumarsäure aus nachwachsenden Rohstoffen
- Entwicklung neuer Enzyme für die Hydrolyse von agrarischen Reststoffen
- Einsatz der maßgeschneiderten Enzympräparate zur fermentativen Herstellung von Fumarsäure
Optimierung der Itakonsäure-Produktion durch Pilze für die Kunststoffproduktion
- Entwicklung und Optimierung der Itaconsäureproduktion
- Untersuchung des Einflusses von Kompartimentierung auf den Stoffwechselweg
- Charakterisierung der Transmembrantransporteffekte
- Entwicklung eines verbesserten Produktionsstamms mit erhöhter Toleranz
Synthese von Menthol aus Zitrusfrüchten
- Entwicklung einer Technologieplattform auf Basis des Bakteriums Pseudomonas putida
- Etablierung einer nachhaltigen und ressourceneffizienten Produktion von oxyfunktionalisierten Monoterpenoiden
- Erarbeitung biotechnologischer Nutzungswege für nachwachsende Rohstoffe (Limonen und Glycerin)
- Ersetzung eines petrochemischen Prozesses durch einen biotechnologischen Prozess zur Produktion von Menthol und Geraniumsäure
Videos
Ein Netz aus Wärme
Mit dem Aufruf des Videos erklären Sie sich einverstanden, dass Ihre Daten an YouTube übermittelt werden und dass Sie die Datenschutzerklärung gelesen haben.
Mit Abwasser Energie erzeugen
Mit dem Aufruf des Videos erklären Sie sich einverstanden, dass Ihre Daten an YouTube übermittelt werden und dass Sie die Datenschutzerklärung gelesen haben.
Aufarbeitung
Gute Praxis
Integrierte Prozessentwicklung
In der Aufbereitungsstufe (Downstream Processing) werden die während der Biokonversion entstandenen Produkte mit dem Ziel aufgereinigt, eine bestimmte Produktreinheit (Produktkonzentration) zu erzielen. Die Produkte liegen in der Regel verdünnt in einer Lösung vor. Sie müssen aufkonzentriert und von nicht gewünschten Stoffen (z. B. nicht umgesetzten Reaktanten, Nebenprodukten, Zellen) abgetrennt werden [Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB (kein Datum), S. 5]. Die Produktaufbereitung ist meistens sehr energieintensiv und beansprucht in der Regel die Hälfte der Betriebskosten eines Bioprozesses. Daher beeinflusst der Produktaufbereitungsprozess den Gesamtenergieverbrauch und die Wirtschaftlichkeit des biotechnologischen Herstellungsverfahrens maßgeblich. Deshalb sind hier Potenziale für die Reduktion des Energieverbrauchs verortet. Durch eine integrierte Prozessentwicklung können Energieeinsparungspotenziale genutzt werden [Nusser, M. et al. (2007), S. 64]. Die Gestaltung des Bioprozesses, insbesondere die Auswahl des Biokatalysators, bestimmt u. a. der Aufwand für die Produktreinigung. Je effektiver ein Biokatalysator Stoffe umsetzt (z. B. hoher Umsatz, wenige bis keine Nebenprodukte), desto weniger Aufreinigungsbedarf entsteht.
Quelle(n):
- Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB (kein Datum): Industrielle Biotechnologie – Die Natur als chemische Fabrik. Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB, Stuttgart [abgerufen am: 07.01.2020], verfügbar unter: Link
- Nusser, M.; Hüsing, B. und Wydra, S. (2007): Potenzialanalyse der industriellen, weißen Biotechnologie. Fraunhofer-Institut für System- und Innovationsforschung (Fraunhofer ISI), Karlsruhe.
Prozessintegration
Die Integration von Reaktion (Biokonversion) und Trennprozessen (Produktaufbereitung) in einem Apparat birgt ein hohes Maß an Energie- und Materialeffizienz [Fraunhofer IGB, IME, IAP, ICT, IPA, UMSICHT, IVV, WKI (kein Datum), S. 11]. Ein Vorteil ist die durch kontinuierliche Abtrennung von Produkten hervorgerufene Verschiebung des Reaktionsgleichgewichts hin zu höheren Umsätzen. Ein weiterer Vorteil erschließt sich durch den prinzipiell geringeren Materialaufwand des integrierten Reaktions- und Trennapparates verglichen mit zwei separaten Apparaten.
Quelle(n):
- Fraunhofer IGB, IME, IAP, ICT, IPA, UMSICHT, IVV, WKI (kein Datum): Vom Rohstoff zum Produkt – Industrielle Biotechnologie in der Fraunhofer-Gesellschaft. Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. [abgerufen am: 19.11.2019], verfügbar unter: Link
Verfahren
Die Entwicklung und der Einsatz von innovativen und effizienten Aufbereitungsverfahren und Verfahrenskombinationen können zur Absenkung des Energieverbrauchs sowie zur Erfüllung der hohen Anforderungen an die Produktreinheit und den Erhalt der Stoffeigenschaften im Bioprozess maßgeblich beitragen [Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB (kein Datum), S. 5]. Zu den vielversprechenden innovativen Verfahrensansätzen werden Elektrodialyseverfahren, Membranverfahren, Destillation und Nanofiltration gezählt [Nusser, M. et al. (2007), S. 64]. Insbesondere die Kombination aus herkömmlichen und innovativen chemischen, thermischen und mechanischen Trennverfahren birgt ein hohes Ressourceneffizienzpotenzial. Beispielsweise kann der Einsatz von innovativen Membranverfahren mit herkömmlichen Trennverfahren wie Zentrifugation, Rektifikation, Extraktion oder chromatographischen Verfahren kombiniert werden [Fraunhofer IGB, IME, IAP, ICT, IPA, UMSICHT, IVV, WKI (kein Datum), S. 10 f.].
Quelle(n):
- Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB (kein Datum): Industrielle Biotechnologie – Die Natur als chemische Fabrik. Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB, Stuttgart [abgerufen am: 07.01.2020], verfügbar unter: Link
- Fraunhofer IGB, IME, IAP, ICT, IPA, UMSICHT, IVV, WKI (kein Datum): Vom Rohstoff zum Produkt – Industrielle Biotechnologie in der Fraunhofer-Gesellschaft. Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. [abgerufen am: 19.11.2019], verfügbar unter: Link
- Nusser, M.; Hüsing, B. und Wydra, S. (2007): Potenzialanalyse der industriellen, weißen Biotechnologie. Fraunhofer-Institut für System- und Innovationsforschung (Fraunhofer ISI), Karlsruhe.
Projekte
Biokonversion von Fettsäuren heimischer Ölpflanzen zu bioaktiven Naturstoffen für Lebensmittel-, Kosmetik- und Pharmaindustrie
- Entdeckung von ruhenden Hefezellen als Biokatalysator zur Synthese von Grünnoten (aldehyd-basierten Aromastoffen im Lebensmittelbereich)
- Biokatalytisches Verfahren als effiziente Alternative zum konventionellen Verfahren
- Untersuchung verschiedener Verfahren zur Gewinnung der Aldehyde aus dem Produktgemisch (Produkt, Edukt, Biokatalysator)
- Aussichtsreichstes Verfahren zur Produktgewinnung: Ausstrippen der flüchtigen Aldehyde und die Adsorption an hydrophobe Harze mit anschließender ethanolischer Extraktion
Microtools for downstream processing
- Entwicklung einer mikroskaligen Downstream-Verarbeitungs-Toolbox, welche Trennprozesse auf Basis von Extraktion, Pervaporation, Adsorption, Absorption und Membrantechnologie beinhaltet
- Schnelle und genaue Generierung von Daten zu Downstream-Prozessen durch Online-Messungen und Experimentierprotokolle
- Durchführung von Experimenten im Labor- und Pilotmaßstab zur Bewertung der Toolbox-Ergebnisse
- Entwicklung von Separationsprozess-Abläufen von Transketolase und Transaminase zur Demonstration der praktischen Anwendbarkeit der Toolbox
Optimierung des downstream processings biologischer Makromoleküle durch Ausnutzung physikalischer Stoffgrößen
- Optimierung der chromographischen oder adsorptionsbasierten Aufbereitung von Proteinlösungen durch verbesserte Auswahl von Adsorbentien
- Reduzierung der Experimente zur Bestimmung des Retentionsverhaltens (Adsorptionsisothermen) durch Verbesserung der Vorhersagbarkeit der Gleichgewichte aus den Reinstoffdaten der festen Phase und der Proteine
- Ermittlung von Henry-Isothermen von Proteinen an kommerziellen hydrophoben Matrices unter verschiedenen Bedingungen
- Charakterisierung heterogener Oberflächen mit Hilfe der Adsorption molekularer Sonden
Videos
Ein Netz aus Wärme
Mit dem Aufruf des Videos erklären Sie sich einverstanden, dass Ihre Daten an YouTube übermittelt werden und dass Sie die Datenschutzerklärung gelesen haben.
Herstellung biobasierter Produkte
Gute Praxis
Produkt- und Anwendungsentwicklung
Für die aus industriellen biotechnologischen Verfahren erhaltenen Zwischenprodukte, oftmals Plattformchemikalien, muss ein Konzept für den anschließenden Wertschöpfungsweg hin zum biobasierten Produkt für den Endverbraucher bereitstehen. Voraussetzung hierfür ist ein Verständnis für die Kundenbedürfnisse und Marktbedingungen der entsprechenden Zielmärkte. Dafür ist es wichtig, dass Unternehmen, die industrielle biotechnologische Produktionsverfahren betreiben, mit den nachfolgenden verarbeitenden Unternehmen der biotechnologisch hergestellten Zwischenprodukte (Kundenunternehmen) intensive Kontakte pflegen und Anforderungen an die Produkteigenschaften abklären. Biotechnische Verfahren und Zwischenprodukte sollten so kundenorientiert wie möglich entwickelt werden, so dass diese im betrieblichen Alltag des Kundenunternehmens zuverlässig verwendbar sind sowie entsprechend den vorliegenden Stoffeigenschaften mit einem oder mehreren geeigneten Verfahren hin zum biobasierten Endprodukt verarbeitet werden können [Nusser, M. et al. (2007), S. 64 f.], denn biobasierte (Zwischen-)Produkte können zum Teil andere stoffbezogene Eigenschaften verglichen mit ihren fossilbasierten Pendants aufweisen. Das wiederum kann in einem veränderten Verarbeitungsverhalten mit geänderten Gebrauchseigenschaften resultieren. Dies bildet die Voraussetzung für eine ressourceneffiziente Verarbeitung biotechnologisch hergestellter Zwischenprodukte hin zu einem biobasierten Endprodukt.
Quelle(n):
- Nusser, M.; Hüsing, B. und Wydra, S. (2007): Potenzialanalyse der industriellen, weißen Biotechnologie. Fraunhofer-Institut für System- und Innovationsforschung (Fraunhofer ISI), Karlsruhe.
Verfahrens- und Produkteigenschaften
Die Erarbeitung der technologischen Grundlagen der Verfahrensstufen sowie die Identifizierung geeigneter Prozessparameter für die Herstellung von Biomaterialien bilden die Voraussetzungen für material- und energieeffiziente Herstellungsverfahren [Fraunhofer IGB, IME, IAP, ICT, IPA, UMSICHT, IVV, WKI (kein Datum), S. 12].
Bei biobasierten Polymer-Produkten können die chemische Struktur der Monomer-Komponenten, das Verarbeitungsverhalten und die Gebrauchseigenschaften bestimmt werden. Daher lassen sich die Produkteigenschaften durch Kombination verschiedener Monomere auf einsatzspezifische Anforderungen einstellen [Fraunhofer IGB, IME, IAP, ICT, IPA, UMSICHT, IVV, WKI (kein Datum), S. 12].
Quelle(n):
- Fraunhofer IGB, IME, IAP, ICT, IPA, UMSICHT, IVV, WKI (kein Datum): Vom Rohstoff zum Produkt – Industrielle Biotechnologie in der Fraunhofer-Gesellschaft. Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. [abgerufen am: 19.11.2019], verfügbar unter: Link
Projekte
Aus CO2 Schmierstoffe herstellen
- Produktion von Schmierstoffen (u.a. für Kraftfahrzeuge) aus CO2 mithilfe von Algen und Hefen
- Bau eines speziellen Photobioreaktors für die Kultivierung von Algen und CO2-Versorgung aus Verbrennungsmotoren
- Einsatz gebildeter Lipide in Sitzschienen von Autos
Dampfsterilisator mit Wärmerückgewinnung
- Ersatz herkömmlicher Dampfsterilisatoren durch innovative Autoklaven für die Abwärmenutzung bei der Produktion hochreiner Biomaterialien
- Kopplung der mit Kühlkreisläufen und Wärmetauschern ausgestatteten Autoklaven mit der Wärmerückgewinnungsanlage des Unternehmens
- Reduktion des Wasserverbrauchs von rund 1600 l auf 15 l und Stromverbrauchs von rund 13 kWh auf 9 kWh pro Zyklus
- circa 80 % Rückgewinnungsrate von thermischer Energie und Verringerung der Prozesszeit auf 70 Minuten pro Zyklus
Kostengünstige Textilien aus Biopolymeren
- Entwicklung von stärkebasierten Textilstrukturen (Geotextilien, medizinische Textilien, gestrickte Pullover)
- Chemische und physikalische Modifikation von Stärke
- Herstellung von Stärke-Biopolymer-Blends
- Demonstratorentwicklung durch Vlieslegung und Stricken
Neue Produkte aus der Insektenbioraffinerie
- Untersuchung der Marktfähigkeit verschiedener Produkte aus Insektenlarven
- Fettanteil u.a. geeignet Kokos- und Palmkernöl zu ersetzen
- Proteinanteil u.a. geeignet zur Herstellung von Klebstoffen, Bindemitteln, Beschichtungen und Verpackungsfolien
O4S – Organic for surfactants
- Verfahrensentwicklung zum Herstellen nachhaltiger Biotenside
- Entwicklungsarbeit im Projekt adressiert die gesamte Prozesskette:
- Bereitstellung passender organischer Rohstoffe (bevorzugt) aus Abfallströmen
- Prozessentwicklung zur Tensidherstellung
- Produktaufarbeitung und -charakterisierung
- Einbindung der Biotenside in naturkosmetische Produkte - Etablierung und Optimierung eines Fermentationsprozesses zur Herstellung der Biotenside Mannosylerythritol-Lipid (MEL) und Cellobiose-Lipid (CL)
- Ersetzen herkömmlicher Substrate für den Fermentationsprozess durch Verwenden von Abfallströmen aus biologischer Landwirtschaft
- Entwicklung eines nachhaltigen industriellen Konzepts mit hohen Raum-Zeit-Ausbeuten
Synthese biobasierter Hochleistungs-Polyamide aus biogenen Reststoffen
- Forschungsteam hat neue Polyamid-Familie entdeckt
- Lässt sich aus einem Nebenprodukt der Zelluloseproduktion herstellen
- Endprodukt hat hohe Temperaturbeständigkeit und ist sowohl transparent als auch teilkristallin möglich